Ensure Flavor & Compliance: A Guide to Testing Vanillin/Ethyl Vanillin
In the food Et en plusbeverage industry, a consistent, authentic dairy aroma is key to a product's market success....... La vanilline and ethyl vanillin serve as indispensable flavor cores in Produits laitiers, baked goods, beverages, and edible oils, making their quality and compliance critically important. Currently, with increasingly stringent food safety regulations (such as the GB2760 standard) and growing consumer demand for ingredient transparency, precisely controlling the use of vanillin-based additives has become a core challenge in product development and quality control within the industry.
Research indicates that while vanillin compounds impart appealing flavors to foods, excessive intake poses potential health risks. Consequently, regulatory bodies worldwide have established strict limits on their addition in various foods—particularly infant and toddler products. This underscores that your choice of vanillin supplier impacts not only flavor but also directly influences product compliance and safety.
Precise detection is essential for ensuring compliance. Currently, the industry predominantly employs methods such as High-Performance Liquid Chromatography (HPLC), Gas Chromatography (C/c), and higher-precision tandem mass spectrometry (LC-MS/MS, C/c-MS/MS) for component monitoring. While each method has its specific applications and precision levels, one universal truth remains: low-purity raw materials with high impurity content significantly interfere with test results, potentially leading to misjudgments and unnecessary compliance risks for your products.
Green Spring Technology deeply understands your pain points. We are committed to providing customers with vanillin and ethyl vanillin powder featuring high purity, low impurities, and exceptional batch consistency. Our ingredients not only deliver pure aroma and outstanding application performance but also ensure the accuracy and reliability of testing data from the source. This enables seamless quality control processes for your products and effortless compliance with regulatory requirements.
Green Spring Technology provides more than just Vanilline en poudreingredients—we deliver peace of mind and reliability. Next, we will systematically analyze the characteristics of different testing methods and offer selection recommendations to help you manage product quality more scientifically. Learn More About Our Comprehensive Solution for Vanillin Powder.

1 Méthodes de détection for Vanillin and Ethyl Vanillin
1.1. - le système High-Performance Liquid Chromatography (HPLC)
HPLC, renowned for its speed and efficiency, is a widely adopted method for detecting vanillin and ethyl vanillin content in food. Utilizing UV or diode array detectors with external standard quantification, it is suitable for food or beverage samples with relatively simple matrices.
In practical applications, optimizing extraction methods and chromatographic conditions can further enhance detection efficiency and accuracy. Research has demonstrated that method optimization achieves high recovery rates and low bias for vanillin and ethyl vanillin in liquid Boisson gazeuses, with a detection limit reaching 0,5 0,5 0,5 0,5 0,5 mg·kg⁻¹. However, for complex matrix samples such as Préparations pour nourrissons powder and dairy products, HPLC is susceptible to interference and requires appropriate purification steps.
Common pretreatment techniques include protein precipitation and solid-phase extraction purification. In Préparations pour nourrissons testing, zinc acetate protein precipitation combined with solid-phase extraction column purification effectively reduced matrix interference. Another dairy study employed n-hexane defatting purification, significantly enhancing method sensitivity with a detection limit of 0.06 mg·kg⁻¹. These practices demonstrate that optimizing pretreatment procedures for different sample matrices is crucial for ensuring detection accuracy.
1.2. - High-Performance Liquid Chromatography-Tandem Mass Spectrometry
High-performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) has become the key technique for detecting vanillin and ethyl vanillin in food due to its high sensitivity, selectivity, and rapid analysis capabilities. This method combines the efficient separation of liquid chromatography with the precise qualitative and quantitative capabilities of mass spectrometry, significantly enhancing the reliability of testing complex food samples.
Studies demonstrate that HPLC-MS/MS performs excellently across diverse food matrices including milk, ham, melon seeds, and rice. It enables broad-spectrum detection of vanillin and ethyl vanillin with detection limits as low as 0.015–0,02 0,02 0,025 mg·kg⁻¹. Single-injection analysis requires only approximately 6 minutes, with recovery rates consistently stable between 75.8% and 116% and excellent repeatability.
Compared to high-performance liquid chromatography (HPLC), HPLC-MS/MS offers significant advantages in detection limits and efficiency: detection limits in infant formula are improved by 5–10-fold, and analysis time is reduced by nearly 40%. Even in high-fat samples like Huile végétales, combining purification techniques such as EMR-Lipid effectively removes matrix interference. Detection limits exceed national standards, meeting the demand for rapid and precise testing across diverse food products.
1.3 chromatographie en phase gazeuse
Gas chromatography (C/c) is widely used for detecting vanillin and ethyl vanillin in food due to its ease of operation, stability, and high sensitivity. It is particularly suitable for analyzing volatile, thermally stable organic compounds.
This method, combined with appropriate pretreatment techniques, can effectively process complex food samples. For instance, in rice noodle testing, the GC internal standard method enables accurate determination with spiked recovery rates ranging from 92.56% to 99.36%, meeting national standard requirements. For high-protein samples like Lait de coco, purification via diatomaceous earth solid-phase extraction yields recovery rates between 95.3% and 110,5 0,5 0,5 0,5 0,5%, with detection limits of 0,2 0,2–0.5 mg·kg⁻¹. For ethanol-containing samples (e.g., yellow wine), combining nitrogen blow-down alcohol removal with solvent extraction yields stable recovery rates of 99.37%–103,3 et 42%, demonstrating excellent repeatability and sensitivity.
Given its broad applicability and reliable results, gas chromatography has become a practical and efficient analytical method for vanillin detection in food.
1.4 Gas Chromatography-Tandem Mass Spectrometry
Gas chromatography-tandem mass spectrometry (GC-MS/MS) offers high sensitivity, strong interference resistance, and precise quantification, making it the mainstream technique for detecting trace vanillin and ethyl vanillin in complex foods. It is particularly suitable for complex matrices such as high-fat and high-protein samples.
This method is often combined with advanced pretreatment techniques to enhance detection efficiency and accuracy. For instance, in Thé au lait analysis, combining headspace solid-phase microextraction (HS-SPME) enables efficient solvent-free extraction. Detection limits for vanillin and ethyl vanillin reached 0.05 mg·kg⁻¹ and 0.03 mg·kg⁻¹ respectively, with recovery rates between 89% and 105%, demonstrating both accuracy and environmental sustainability.
In dairy product testing, Multi-Reaction Monitoring (MRM) mode further enhances sensitivity, achieving a quantitative limit of 0.02 mg·kg⁻¹ for vanillin in Cow& ' S lait. The method exhibits excellent linearity (R² ≥ 0.9998) across the 0,1 0,1 0,1 0,1 0,1 0,1–4.0 mg·L⁻¹ range with stable recovery rates at low concentrations. Compared to traditional GC methods, GC-MS/MS offers fourfold higher detection sensitivity, making it more suitable for trace detection and false positive screening.
Continuous innovations in pretreatment techniques, such as “liquid-liquid extraction-solidification counter-extraction,” further simplify operations and enhance sensitivity, achieving a vanillin detection limit of 0,004 0,004 0,004 mg·kg⁻¹ in milk powder.
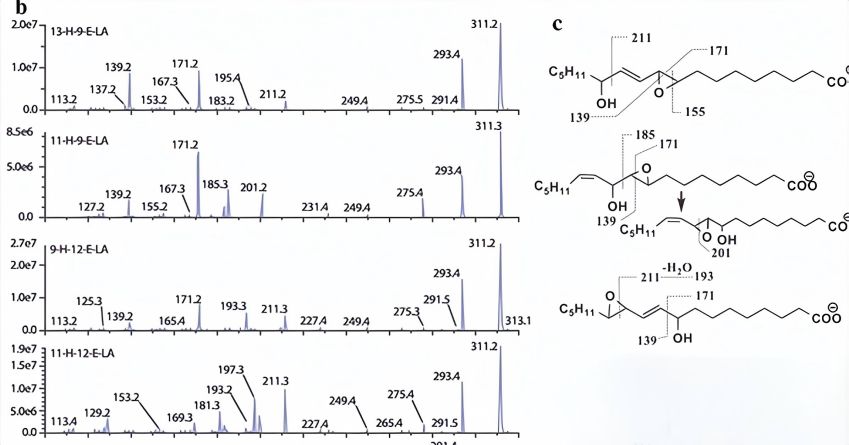
With its outstanding interference resistance and trace detection capabilities, GC-MS/MS provides reliable support for food safety regulation and corporate quality control.
1.5 Electrochemical Methods
Electrochemical methods are fast, sensitive, and cost-effective, widely applied for rapid screening and quantitative detection of vanillin and ethyl vanillin in food. This approach analyzes the relationship between electrical signals and analyte concentration, commonly employing techniques like voltammetry and potentiometric analysis.
In practical applications, this method demonstrates outstanding performance. For instance, in chocolate ethyl vanillin detection, a Nafion-graphene-modified electrode combined with differential pulse voltammetry enables detection within one minute. The linear range spans 2.4–8.2 µg·mL⁻¹, with a detection limit of 0.076 µg·mL⁻¹ and recovery rates ranging from 98.6% to 101.38%. For vanillin detection in Les cookies, the graphene/cobalt tetroxide sensor exhibited excellent linearity (R² = 0.997) over 0.1–80 µmol·L⁻¹, with a detection limit of 0.033 µmol·L⁻¹ and an average recovery rate of 102.4%.
Electrochemical methods require no complex pretreatment and involve significantly lower equipment costs than chromatographic techniques, while their sensitivity meets routine detection requirements. Despite challenges such as limited sensor lifespan and complex modification processes, their high efficiency and cost-effectiveness confer broad application potential in rapid food testing.
1, 6, 6 Capillary Electrophoresis
Capillary electrophoresis (CE CE CE CE) offers high efficiency, rapidity, and environmental friendliness, making it suitable for the rapid detection of vanillin and ethyl vanillin in food. This method utilizes an electric field to separate target compounds within a capillary tube, featuring simple sample preparation and minimal solvent consumption, particularly well-suited for complex food matrices like candies and beverages.
Research indicates CE performs well in various food detection applications. For instance, in the accurate determination of vanillin content in Da Bai Tu milk candy, a single analysis can be completed within 3–8 minutes under optimized conditions. The linear range spans 5.0×10⁻⁶ to 1.0×10⁻³ g·mL⁻¹, with a detection limit of 0.25–10 µg·mL⁻¹. Spiked recovery rates typically range from 85% to 108%, meeting routine testing requirements.
CE also enables simultaneous multi-component analysis, such as concurrent detection of caffeine, vanillin, and ethyl vanillin in beverages within 3 minutes. Despite potential interference in complex samples, its high resolution, low cost, and environmental advantages make it a promising technique for vanillin detection in food.
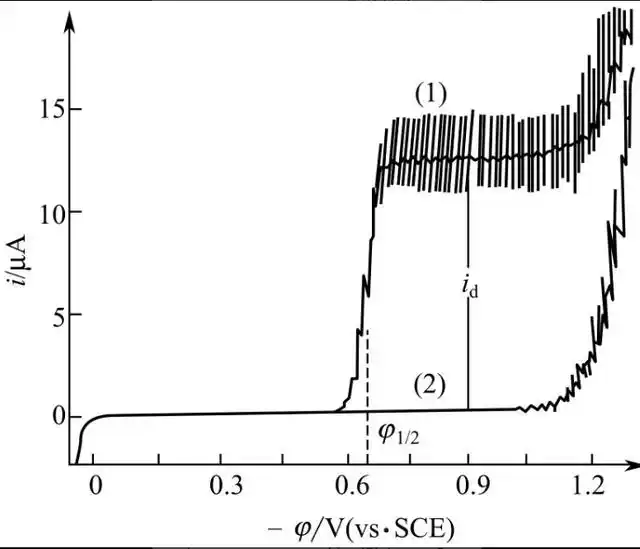
1.7 Alternative Detection Methods
Beyond mainstream techniques like chromatography and mass spectrometry, various rapid detection technologies have emerged in recent years, offering new options for identifying vanillin and ethyl vanillin in food.
UV spectrophotométrie is simple and low-cost, suitable for rapid screening of high-concentration samples. However, it cannot distinguish between vanillin and ethyl vanillin, limiting its application. Surface-Enhanced Raman Spectroscopy (Les SERS) is portable, rapid, and possesses fingerprint identification characteristics, enabling on-site detection in samples like milk powder. Analysis is completed within 5 minutes with a detection limit of 10 µg·mL⁻¹, demonstrating strong practicality. Fourier Transform Infrared Spectroscopy (FT-IR) exhibits excellent interference resistance and fast scanning speed, performing well in complex matrices such as milk powder and being suitable for rapid screening of dairy products.
These methods expand the detection options for vanillin, providing more feasible solutions for on-site quality control and rapid screening in the food industry.
Tableau 1 dosage de la vanilline et de l’éthyl-vanilline dans les aliments
Matrice d’échantillon |
Méthode de Purification |
Detection Methods | Méthode limite de détection (mg- kg-1) | Taux de recouvrement (%) | RSD (%) | Temps de chargement d’une seule aiguille (min) | Références: |
soft drink |
QuEChERS modifiés |
HPLC-UV |
0.5 |
96,7 à 100,4 |
3.53~4.70 |
12 | [16] [traduction] |
Préparations en poudre pour nourrissons | Oasis MAX nettoyage de colonne d’extraction en Phase solide |
UPLC-UV |
0.1 |
84,0 ~ 93,3 |
5,2 à 6,2 |
10 | [17] [traduction] |
Lait de soja | / | HPLC-UV | 0.04~0.18 | 63.39~88.73 | 0,9 ~ 4,5 | 42 | [18] [traduction] |
dairy products | Purification de dégraissage Hexane | HPLC-UV | 0,06 0,2 | 80,4 à 110,0 | 1.66~9.52 | 35 | [19] [traduction] |
Lait, jambon, melon Riz, riz, boissons. Et pâtisseries | Style - SCREENRSSH2P Phase solide Nettoyage de la colonne d’extraction | UPLC- MS/MS |
0,075 ~ 0,090 |
75,8 ~116 |
1.58~6.01 |
6 |
[4] [traduction] |
vegetable oil | Emr-lipide Purification | UPLC- MS/MS | 0,035 ~ 0,0376 | 72.8~91.8 | 1.6 à 8.6 | 8 | [21] [en] |
vermicelle | / | GC | 2.2. - | 92.56~99.36 | 2.21~2.48 | 30 | [23] [en] |
coconut milk | Terre diatomée extraction en phase solide purification sur colonne | GC | 0,2 ~ 0,5 | 95,3 à 110,5 | 1.2~2.5 | 25 | [24] [traduction] |
" vin jaune " (vin de riz chaud, généralement servi chaud) | / | GC | 0.2 | 99.37~103.32 | 2,22 à 3,67 | 25 | [25] [traduction] |
milk tea | / | Cg/em | 0,03 ~ 0,05 | 88.99~105.15 | 2.40~9.26 | 27 | [28] [traduction] |
cow's milk | / | Cg/em | 0.02 | 79,1 à 86,2 | 3.3 | 60 | [29] [en] |
Les boissons | Purification de colonne noir de carbone graphitisé | Cg/em | 0.5 | 81~110 | 2,4 à 5,6 | Taux de croissance annuel | [30] [en] |
infant formula | Phase d’acceptation durcissement - Extraction inverse | Cg/em | 0.004 | 82,0 ~ 98,0 | 2.83~6.83 | 24 | [31] [en] |
chocolats | / | Méthode électrochimique | 0,076 µg- mL-1 | 98.60 à 101.38 | 1.6 | 1 à 2 | [33] [traduction] |
chocolats | / | Méthode électrochimique | 6,7 × 10-7 mol- L-1 | 99,3 ~ 102,1 | 3.2. - | / | [34] [traduction] |
cookies | / | Méthode électrochimique | 0,033 µmol- L-1 | 100,8 à 103,8 | Taux de croissance | / | [35] [traduction] |
Le caramel | / | CE | / | >95 | <2.8 | 20 | [37] [traduction] |
chocolats | / | CE | 3,87 × 10-7 g - mL-1 | 96,5 ~ 108,2 | 1.7~2.8 | 10 | [38] [traduction] |
Boissons, gelées, conserves | / | CE | 1 µg - mL-1 | 90.3~95.9 | 2.85~4.43 | 8 | [39] [traduction] |
Flocons d’avoine | / | spectrophotometry | 2.2206 × 10-2 g - L-1 | 101.8-101.8-101.8 | 0,44 0,44 0,44 | / | [41] [traduction] |
infant formula | / | SERS | 10 µg- mL-1 | 80.5~86.9 | < 8,6 | 5 | [42] [traduction] |
2 Technology Safeguards Quality, Green Spring Helps You Move Forward Steadily
En aujourd’hui's world, where food flavor and safety are equally important, selecting appropriate detection methods for vanillin and ethyl vanillin is key for enterprises to achieve product quality control and compliance. Currently, chromatography and chromatography-mass spectrometry (MS) technologies dominate due to their high sensitivity and accuracy, with LC-MS/MS demonstrating significant advantages in complex food matrices. Emerging techniques like electrochemical detection, capillary electrophoresis, and Raman spectroscopy also offer flexible, efficient complementary solutions for rapid screening and on-site testing.
Green Spring Technology deeply understands enterprises' multifaceted needs regarding flavor consistency, detection reliability, and compliance safety. Our vanillin powder and ethyl vanillin raw materials are consistently produced using advanced quality control technologies like LC-MS/MS. We rigorously monitor the purity and impurity levels of each batch to ensure outstanding batch consistency and minimal interference. This not only helps customers enhance detection accuracy and reduce misjudgment risks but also streamlines your quality control processes, accelerates product launches, and enables confident compliance with various regulations and market sampling inspections.
Choosing Green Spring Technology means selecting not just a premium ingredient, but also the peace of mind and trust born from technological innovation.
Contact us today at helen@greenspringbio.com or WhatsApp: +86 13649243917 to request complimentary samples and technical documentation—infuse your products with the taste of stability and the assurance of safety!
Références:
[1] Walton N J, Mayer M J, Narbad A. Vanillin[J]. Phytochemistry, 2003, 63(5):505-515.
[2] LIU Xiangping, HUANG Wei. Dosage simultané de la méthyl vanilline et de l’éthyl vanilline dans les aliments par chromatographie liquide à haute performance [J]. Chinese Journal of Preventive Medicine, 2006, 40(004):296-297.
[3] NI Y on g NI an, ZHANG Gu ow en, KOKO T S. Détermination spectrophotométrique simultanée du maltol, de l’éthyl maltol, de la vanilline et de l’éthyl vanilline dans les aliments par étalonnage multivarié et réseaux neuraux artificiels [J]. Food Chemistry, 2005, 89: 465-473
[4] YANG Huamei, HANG Li. Détermination simultanée de quatre arômes couramment utilisés dans les aliments par chromatographie liquide ultra performance — spectrométrie de masse tandem [J]. Chromatography, 2015, 33(3):250-255.
[5] Xuemei Sun, Qiang Xu, Xiaomeng Sun, et al. Détermination simultanée de la vanilline et de l’éthyl-vanilline dans les boissons lactées par chromatographie liquide haute performance [J]. Journal of Food Safety and Quality Testing, 2020, 11(17):6023-6027.
[6] Commission nationale de la santé et de la planification familiale du peuple et#39; S république de Chine, State Food and Drug Administration. Norme nationale pour la sécurité alimentaire: GB 2760-2014 [S]. Beijing: China Standard Press, 2014.
[7] Richard, D, Thompson et coll. Détermination de la coumarine comme adultérant dans les produits d’aromatisation de la vanille par chromatographie liquide à haute performance [J]. Journal of Chromatography A, 1988, 438(1):369-382.
-
Précédent précédent
Isomaltooligosaccharide: Empowering Functional Foods for Health and Flavor Enhancement
-
Suivant:
De quoi est faite la vanilline?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais



