Quelles sont les utilisations du D Tagatose?
D tagatose is a monosaccharide with special health benefits that was discovered in recent years. It was determined to be Generally Recognized as Safe (GRAS) Par:the US Food Et en plusDrug Administration (FDA/FDA) in 2001. Studies have shown that D-tagatosenot only has similar taste Et en plusphysical properties to sucrose1), and can be used as a sweetener to replace sucrose, but also has a complementary therapeutic effeton the treatment De ladiseases in specific populations (2), so it is currently attracting a lot De laattention À partir dethe market and consumers. In view De lathis, it is De lagreat significance to make full use of the superior properties of D-tagatoseand apply it to the fields of food, medicine, cosmetics, etc.
1 Structure et propriétés physiques et chimiques de D-tagatose
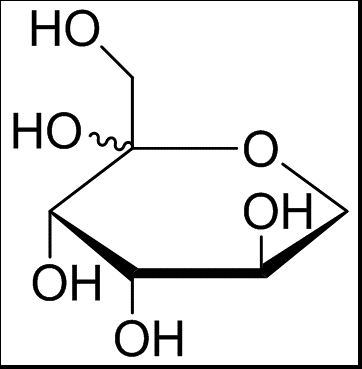
D tagatose is a rare natural hexopyranose, an isomer of D-galactose, and a reverse D-fructose diastereoisomer at the C-4 position (as shown in Figure 1(3)). According to the Lobry de Bruyn-Al- berda van La transformation d’ekenstein, le D-talose et le d-tagatose dans la figure peuvent s’interconvertir entre eux en raison de l’atome de carbone α de la molécule de sucre fournissant de l’hydrogène actif pour donner un groupe carbonyle, résultant en une forme d’enol, dans une solution alcaline. D-Tagatose est un cristal blanc poudré sans odeur. Sa formule moléculaire est CgH, le poids moléculaire 180,16, le point de fusion 132° C-135 °C et une solution aqueuse à 1% [α]20-6±1° (C =5,H₂O); le D-Tagatose est résistant aux acides et peut exister de façon stable à pH 3~7. Il est également résistant à la chaleur et aux alcalis. Elle est sujette au brunissement Maillard et peut être caramélisée à des températures plus basses.
2 D-Tagatose propriétés fonctionnelles
2.1 inhibe l’hyperglycémie
D-Tagatose is a low-energy sugar with a sweetness that is about 92% that of sucrose, and it is not well absorbed by the body (4). Donner Thomas et al. (2) used 6 healthy people and 6 non-insulin-dependent diabetes mellitus patients as research subjects, and measured the changes in blood glucose and insulin levels after they were given 75 g of glucose or 75 g of D-tagatose orally over a period of 3 hours, or 75 g of tagatose orally pour30 minutes followed by 75 g of glucose.
Les résultats ont montré que l’administration orale de D-tagatose seule ne provoquait pas de changements dans les taux de glycémie et d’insuline chez les personnes en bonne santé et les patients atteints de diabète de type 2. Au contraire, il a réduit l’ augmentation de la glycémie causée par l’ apport de glucose chez les patients diabétiques, mais n’ a pas eu d’ effet significatif sur la sensibilité à l’ insuline des patients diabétiques chez les patients diabétiques de type 2. De même, donner aux patients diabétiques de type 2 75g de saccharose, ou 75g de D-tagatose 30 minutes avant de prendre 75g de saccharose, peut également supprimer l’augmentation de la glycémie causée par le saccharose. Par conséquent, le D-tagatose est considéré comme ayant un effet supplémentaire sur le traitement du diabète de type 2, ce qui peut être parce que le D-tagatose affaiblit l’absorption du saccharose dans l’estomac et les intestins, tout en prédisant efficacement les augmentations de glucose dans d’autres produits de sucre et une augmentation du taux de glucose dans le sang.
2.2 améliore la flore intestinale et favorise la croissance de bactéries bénéfiques
Le D-tagatose est fermenté par des micro-organismes dans le tractus gastro-intestinal humain, produisant principalement de l’acide acétique, de l’acide butyrique et de l’acide hexanoïque, l’acide butyrique étant le composant principal. L’acide butyrique peut favoriser la croissance de bactéries bénéfiques telles que les lactobacilles et est une bonne source de cellules épithéliales du côlon. Il a également un certain effet en inhibant le cancer du côlon et les bactéries pathogènes intestinales. Laerke et al. (5) ont recueilli et analysé les selles de 16 personnes en bonne santé (10 g de D-tagatose ont été administrés trois fois par jour pendant 14 jours) et ont constaté que la concentration de bactéries lactiques dans les selles le 14e jour après l’ingestion était significativement plus élevée que celle sans ingestion, tandis que la concentration de bactéries coliformes dans les selles le 14e jour après l’ingestion était réduite.
2.3 pas facilement décomposé et utilisé par les bactéries orales, et ne cause pas la carie dentaire
In 2002, the US FDA confirmed that D-tagatose is not broken down by oral bacteria and does not cause tooth decay. D-tagatose can also effectively eliminate bad breath and prevent diseases such as gingivitis.
3. Procédé de production de D-tagatose
Le D-tagatose se trouve dans de nombreux aliments, principalement des produits laitiers tels que la poudre de lait stérilisé, le fromage et le yogourt [6]. Actuellement, le D-tagatose est produit par isomérisation du galactose à l’aide de méthodes biologiques et chimiques.
3.1 méthode biologique
Lzumori et al. [78] ont utilisé Mycobacterium smegmatiset Arthrobacter globiformis, et Muniruzzaman et al. [9] ont utilisé des agents d’enterobacter pour convertir le galactitolen tagatose, une méthode utilisant le galactitol pour la biosynthèse du D-tagatose, c’est-à-dire la méthode de biosynthèse du galactitol. En outre, la méthode de synthèse enzymatique est également utilisée dans la production industrielle. Des études ont montré que l’enzyme L-galactose isomérase a une activité catalytique dans le processus de conversion, convertissant le L-galactose en L-ribulose. Puisque l’isomérase de L-galactose est une enzyme relativement spécifique (spécifique au groupe), elle peut convertir l’aldose en kétose. Par conséquent, tout en catalysant le L-tagatose, il peut également convertir d’autres aldose (comme le D-galactose, le DL-fructose et le D-xylose) à la forme hexose correspondante. Si le perméat de lactose est utilisé comme matière première pour la préparation enzymatique du tagatose, le flux de processus est:
Perméat de lactose → ultrafiltration → osmose inverse → microfiltration → hydrolyse → concentration → fermentation → isomérisation → concentration → cristallisation → produit fini.
3.1.1 élimination des protéines, des sels et des substances moléculaires élevées
Les substances hautement moléculaires telles que les protéines sont retirées du perméat de lactose pour empêcher la contamination bactérienne des étapes ultérieures du processus. Les sels, par exemple, inhibent la cristallisation du tagatose au cours de la phase de cristallisation et doivent donc également être éliminés.
3.1.2 hydrolyse
Après l’élimination des substances de poids moléculaire élevé telles que les protéines du perméat de lactose, l’enzyme lactase immobilisée est utilisée pour hydrolyser en continu le lactose en glucose et en galactose. Les conditions d’hydrolyse sont des températures de 40°C à 60°C et un pH de 4 à 6.
3.1.3 Concentration
L’hydrolysat de lactose est concentré en une solution contenant 2 à 20% de galactose et 2 à 20% de glucose, le rapport des deux étant de 1 à 1, le reste étant des protéines, des graisses, du sel et du lactose non digéré.
3.1.4 Fermentation
Le Lactose est hydrolysé pour former un mélange de galactose et de glucose. Après la fermentation sélective par la levure ou les bactéries, le glucose est fermenté en éthanol, tandis que le galactose n’est pas fermenté et entre dans la prochaine étape d’isomérisation, ou le galactose est séparé, évaporé, concentré et cristallisé pour obtenir la poudre de galactose pure.
3.1.5 isomérisation enzymatique
Le bouillon de fermentation est centrifugé ou microfiltré pour enlever les cellules microbien, et distillé pour enlever l’éthanol pour obtenir un concentré de galactose.L-TagatoseEst obtenu par isomérisation avec L-galactose aldéhyde isomérase.
3.1.6 Purification
Le mélange obtenu par isomérisation est séparé par chromatographie sur colonne d’échange de cations et le produit fini est obtenu par concentration et cristallisation.
3.2 méthode chimique
Beadle et al. (10) ont utilisé une méthode chimique en deux étapes pour produire du D-tagatose à partir du galactose. Le Galactose est d’abord isomérisé en complexe d’hydroxyde de métal insoluble tagatose sous catalyse d’un sel de métal alcalin soluble (par exemple, Ca(OH)₂), et le produit final du tagatose est obtenu en neutralisant le complexe avec de l’acide.
3.2.1 isomérisation
L’isomérisation est la formation d’un complexe hydroxide-tagatose métallique, un complexe intermédiaire insoluble, qui est important dans la production chimique de tagatose. (1) la formation d’un complexe intermédiaire insoluble facilite la direction positive; (2) le galactose est instable dans des conditions alcalines et est sujet aux réactions secondaires et aux réactions de dégradation, et la formation du complexe intermédiaire peut inhiber l’apparition de réactions secondaires; (3) le complexe intermédiaire insoluble précipite et peut être efficacement séparé d’autres sous-produits.
3.2.2 neutralisation des acides
Le but de la neutralisation acide est de produire des sels métalliques insolubles pour séparer le tagatose des intermédiaires complexes métalliques.
3.2.3 Purification
La D-tagatose est séparée du système de réaction par cristallisation, tandis que le filtrat contient encore du tagatose. Par conséquent, le filtrat est réagi avec un hydroxyde métallique alcalin pour former un complexe hydroxyde-tagatose métallique pour extraire le tagatose.
Currently, Maryland Biospherics has patented a chemical method for producing tagatose products. Of course, there are also some problems with the chemical production of D-tagatose, such as the use of strongly alkaline metal hydroxides and high pH, which are not conducive to food processing.
4 D-tagatose dans les processus biochimiques humains
4.1 digestion et absorption humaines
Le D-tagatose est principalement digéré et absorbé dans les intestins, mais il y a encore un débat dans la communauté universitaire sur la quantité exacte de digestion et d’absorption. BHKR (4) a utilisé L-rhamnose comme référence pour étudier le corps humain et#39; S absorption de D-tagatose. Étant donné que le taux de diffusion passive des substances à travers la muqueuse intestinale dépend du poids moléculaire et de la lipophilicité, et que la L-rhamnose est un poids moléculaire légèrement inférieur et un composé légèrement plus lipophile, ainsi D-tagatose est légèrement plus absorbé dans l’intestin que la L-rhamnose (14% à 24%). Par conséquent, b[unused_word0006] r estime que le corps et#L’absorption de D-tagatose ne dépassera pas 20%.
Contrairement à b-sp r's report of low D-tagatose absorption, Norman et al. [11 found that D-tagatose absorption in patients with ileostomies could reach 80%. Jenkins et al. (12 ) previously found that L-rhamnose absorption in patients with this operation was close to 50%. Although ileostomy can only provide a limited assessment of incomplete digestion and absorption of monosaccharides, the conclusions of these studies are contrary to those of Bär. Similarly, Buemann et al. (13) found in a double-blind crossover trial that only 1.5% of the 30 g D-tagatose ingested orally was excreted in the urine after 8 individuals had ingested 30 g D-tagatose and 30 g D-fructose alone.
4.2 biotransformation humaine
Le D-tagatose peut être phosphorylé et converti en 1-phospho-D-tagatose dans le corps humain. Raushel & Cleland a signalé [14] que dans des conditions d’atp et de K+, la fructokinase du foie bovin peut catalyser la phosphorylation du D-tagatose pour produire du 1-phospho-D-tagatose. Comme la fructokinase ne se trouve que dans le foie et les reins, le 1-phospho-D-tagatose est également principalement produit dans le foie et les reins, et se forme moins dans les muqueuses intestinales et les cellules des îlots. Buemann et al. [13] ont constaté dans le cadre d’un essai croisé en double aveugle que le phosphore inorganique sérique était temporairement réduit, ce qui peut être directement lié à la formation de 1-phospho-D-tagatose.
Le 1-Phospho-D-tagatose peut continuer à être décomposé par l’aldolase dans le foie pour former du d-glycéraldéhyde et du phosphate de dihydroxypropanone, ce qui conduit à la conversion gluconéogène du D-tagatose en glucose. Rognstad (15.16) a utilisé des cellules de foie de souris et du D-tagatose dans une culture in vitro pour produire du glucose, dans lequel le taux de gluconéogénique de 20 mmol/L D-tagatose était deux fois plus élevé que celui de 20 mmol/L D-galactose et la moitié plus élevé que celui du fructose. "Le C-fructose et ¹⁴C-D-tagatose forment tous deux le glucose lC par la voie gluconéogène, ce qui indique qu’ils ont la même voie gluconéogène.
Bien que la voie gluconéogénique du D-tagatose n’ait pas encore été établie, il est probable qu’il soit métabolisé par la voie de l’acide galactose-phosphorique dans le foie des mammifères. Par exemple, une isomérase catalyse la conversion du 1-phospho-D-tagatose en 1-phospho-galactose. Le tracé isotopique a révélé que l’augmentation du fructose en D-tagatose inhibe la conversion du D-tagatose en glucose, et l’augmentation du D-tagatose en fructose n’affecte pas la gluconéogenèse du fructose. Cela peut être dû au fait que la structure de D-tagatose est plus sujette à la gluconéogenèse que le fructose.
5 applications D-tagatose
5.1 Application dans les aliments
En tant que personnes&#Le niveau de vie continue de s’améliorer, et de plus en plus de gens commencent à prêter attention à leur santé et à manger des aliments à faible teneur en énergie. D-tagatose, en tant que sucre à faible énergie, peut donner plein jeu à ses avantages dans les aliments. Marzur (17) a rapporté qu’en plus d’être faible en énergie, le D-tagatose ne provoque généralement pas de diarrhée pendant la digestion et l’absorption dans le corps humain, ce qui est le cas avec d’autres substituts de sucre composés polyhydroxy. Dans une expérience d’alimentation de trois mois avec des souris, il a été constaté que le poids corporel des souris nourri à 15% (p/p) de saccharose était deux fois plus élevé que celui des souris nourri à 15% (p/p) de D-tagatose. Parce que le D-tagatose est semblable au saccharose dans le goût et les propriétés physiques, et a des propriétés physiques et chimiques telles que la résistance à la chaleur, la résistance aux acides et la résistance aux alcalis, il est largement utilisé comme un édulcorant parfait dans l’industrie alimentaire. Il est principalement utilisé dans la production de chocolat, de produits de boulangerie, de crème glacée, de bonbons durs et mous, de chewing-gum, de boissons gazeuses, de condiments et d’autres produits.
5.1.1 Application dans l’industrie des boissons
In the beverage industry, the main sweeteners added are saccharin, cyclamate, aspartame, acesulfame, stevia and sucralose. These are all strong sweeteners, and sometimes, in consideration of the taste, their The result is a bitter aftertaste, metallic taste and astringent taste. However, Tagatose can effectively reduce these undesirable factors. D-Tagatose has a synergistic sweetening effect, and just a small amount can significantly enhance the sweetness. For example, adding D-tagatose to low-fat milk drinks (chocolate and yogurt flavors) can not only reduce undesirable flavors, but also make the sweetness of the product more stimulating, the flavor more mellow and rich; adding D-tagatose to lemon juice drinks can make the product taste fresher and cleaner; it can also increase the soluble solids content of the beverage system.

Par conséquent, en 2001, la Food and Drug Administration des États-Unis a officiellement approuvé l’utilisation deD-tagatose as a sweetener in the food and beverage industry. It is now widely used in the US as a sucrose substitute in health drinks, yogurt, fruit juice and other products.
5.1.2 Application dans les aliments à base de céréales
Le point de fusion élevé, la résistance à la chaleur, la résistance aux acides et aux alcalis, et la caramélisation à basse température du tagatose sont importants pendant le traitement des céréales. C’est parce que le tagatose a une faible viscosité et est facile à cristalliser. Par conséquent, l’application de glaçage à base de tagatose à la surface des céréales augmente non seulement la douceur du produit, mais prolonge également sa durée de conservation.
5.2 Applications dans la médecine, les cosmétiques et d’autres domaines
En plus de ses excellentes propriétés comme édulcorant dans les aliments et les boissons, le D-tagatose peut également être utilisé comme excipient dans les produits pharmaceutiques et comme humectant et stabilisant dans les cosmétiques. À l’heure actuelle, dans le dentifrice et le rince-bouche, le D-tagatose est principalement utilisé comme agent mouillant, suivi d’un stabilisateur, mais il peut également améliorer efficacement le goût du dentifrice et du rince-bouche. De nos jours, de nombreux dentifrices utilisent du D-sorbitolou de la glycérine, ou une combinaison des deux, comme agent mouillant.

Cependant, la douceur du mélange de D-sorbitol et de glycérine est la moitié de celle du saccharose, et cette douceur n’est pas aussi désirée lors du brossage des dents. Par conséquent, la saccharine, un édulcorant de haute intensité, est ajoutée à de nombreux dentifrices pour rendre le produit aussi bon qu’il le devrait. Cependant, ce composé, tout en offrant la mouillabilité et la douceur requises, a également un goût métallique, un arrière-goût amer et un arrière-goût de saccharine. Le D-tagatose, comme le saccharose, est deux fois plus sucré que le D-sorbitol, et son ajout maintient non seulement la douceur du dentifrice, mais prévient également la carie dentaire. En mesurant l’activité dans l’eau et la teneur en humidité du D-tagatose et du D-sorbitol et en comparant leur mouillabilité, on peut voir à partir des courbes de désorption du D-tagatose et des courbes du D-sorbitol, lorsque le D-tagatose est dissous dans une eau supérieure à 0,62, le D-tagatose et le D-sorbitol sont considérés comme ayant la même mouillabilité en termes d’activité de l’eau. Lorsque le dentifrice est ajouté avec 20% à 25% (p/p) D-tagatose, non seulement la douceur atteint un niveau satisfaisant, mais il maintient également une bonne mouillabilité et stabilité.
At present, although the mechanism of action of D-tagatose as a new monosaccharide in the human body needs to be further explored, its excellent physical and chemical functional properties are undeniable. It is expected that in the next few years, D-tagatose will become a best-selling natural sweetener on the international market, and will be widely used in food, medicine, cosmetics and other fields. Its market prospects are very broad.
Référence:
[1] Sang-Hyun Yoon,Pil Kim,Deok-Kun Oh. Propriétés de L- arabinose isomérase de escherichia colias biocatalyst pour la production de tagatose [J]. Journal mondial de microbiologie& Biotechnology,2003, 19:47-51.
[2] Donner Thomas,Wilber Jean,Ostrowski Debra. D-tagato- se: une nouvelle thérapeutique adjuvant Pour le diabète non insulino-dépendant [J].Diabetics,1996,45(supplément):125A.
[3] Hans Beyer,Wolfgang Watler,Tang Weicheng, manuel de chimie organique [M], Beijing: Higher Education Press, 1989, 306-307.
[4] b
[5] Laerke H.N.,Jensen B.B,Hφjsgaard La plupart du temps. influence De D-tagatose sur la composition bactérienne et la capacité de fermentation d’échantillons fécaux de volontaires humains [J.J.Nutr. , 2000,130:1772-1779.
[6] Lu,Y. humectances of D-tagatose and D-sorbitol [J]. In- international Journal of Cosmetic Science,2001,23(3):175-181.
[7] Izumori K,Tsuzaki K.Production of D-tagatose À partir de D galactitol by mycobactérie smegmatis [J].J.Ferment. Technol.,1988,66:225-227.
[8] Izumori K,Miyoshi T,Tokuda S,et 1.Production of D tagatose de ducitol par arthrobacter globiformis [J].Appl. Environ.Microbiol,1984, 46:1055-1057.
[9] Muniruzaman L,Tokunaga D,Izumori K.Isolation of Fr - terobacter agglomérans souche 22le du sol, une puissante D-ta- gatose Le producteur from galactitol [J].J.Ferment. Bioeng, 1994,78:145-148.
[10] Beadle J.R. Saunders J.P.,Wajada t.j.processus for Fabrication de tagatose [P]. World Patent.12263,1992.
[11] Normen L,Laerke H.N.,Langkilde A.M,et al.petit Absorption bo- wel de D-tagatose et effets apparentés sur le bohydrate de carbone digestibilité [J].Am.J.Clin.Nutr. ,2001,73: 105-110.
[12] Jenkins A.P.,Menzies D.,Nukajam W.S.,etal.The effect De lactulose ingérée lors de l’absorption de la L-rhamnose, du d-xylo-se et du 3-0-méthyl-d-gluose chez des sujets atteints d’iléostomies [J]. Scand.J.Gastroenterol,1994, 29:820-825.
[13] Buemann B,Toubro L,Holst J,et Al.D-Tagatose,a Ste - réoisomère de D-fructose, augmentation de la concentration d’acide urique dans le sang [M].Metabolism,1999.
[14] Raushel F.M.Cleland w.w.bovin foie Fructokinase: purification et propriétés cinétiques [J]. Biochemistry,1977, 16:2169--2175.
[15] Rognstad R.Gluconeogenesis from D-tagatose by isolated rat and Le hamster foie Cellules [J]. Feb - feb Lett. (en anglais) ,1975,52:292-294.
[16] Rognstad r.voie de la gluconéogenèse à partir de tagatose dans les hépatocytes de rat [J].Arch.Biochem.Biophys. ,1982,218: 488-491.
[17] Marzur a.w.substituts fonctionnels du sucre avec caissons réduits [P]. EP 341062,1989.
-
Précédent précédent
Quelle est l’utilisation de la poudre de Tagatose dans le domaine alimentaire?
-
Suivant:
La méthode de synthèse de la poudre de Tagatose D?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




