Quelle est l’utilisation de l’acide hyaluronique sur la peau?
Acide hyaluroniqueEst un polysaccharide commun largement trouvé dans divers tissus du corps humain, y compris le tissu cutané et le tissu conjonctif. Depuis son premier isolement de l’humour vitré bovdanspar Meyer et al. en 1934, diverses fonctions de l’acide hyaluronique ont été découvertes. En raison de son hydrophilicité, viscoélasticité, biocompatibilité, et manque d’immunogénicité, l’acide hyaluronique A atrouvé des applications dans les systèmes topiques d’administration de médicaments, lA acicatrisation des plaies, lA athérapie de barrière pour les maladies, et le traitement des états inflammatoires.
1 propriétés physiques et chimiques
Hyaluronic acid is a linear polysaccharide polymer composed De laD-glucuronic acid and N-acetylglucosamine, with Le conseil des ministresmolecular formula (C₁₄H₂₁NO₁₁)_n. Based on its molecular weight, hyaluronic acid can be classified inÀ propos dehigh-, medium-, and low-molecular-weight types. Most De lathe properties De lahyaluronic acid are related to its molecular weight. High-molecular-weight hyaluronic acid (HMW-hyaluronic acid) hEn tant quea molecular weight range De la103–104 kDa, medium-molecular-weight hyaluronic acid has a molecular weight range of 200–103 kDa, and Acide hyaluronique de faible poids moléculaire (LMW-hyaluronic acid) has a molecular weight range of 10–200 kDa. Through hyaluronidase, mechanical force, oxidative stress, and other regulatory processes of hyaluronic acid degradation and metabolism, high-molecular-weight hyaluronic acid can be degraded into hyaluronic acid polymers (Ou bienfragments) of different sizes. Low-molecular-weight hyaluronic acid can also be de novo synthesised by hyaluronic acid synthase during inflammatory processes [1] [traduction]. In the human body, hyaluronic acid typically exists dansa high-molecular-weight form with a size of approximately 104 kDa. It can bind to water equivalent to 1,000 times its own weight through hydrogen bonds [2] and achieve moisturising effects by reducing water evaporation and inducing hydration of the stratum corneum.
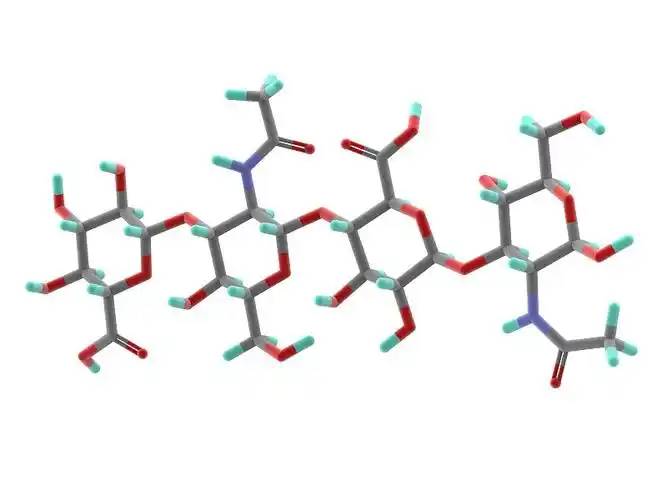
2 propriétés biologiques
2.1 biocompatibilité
Unlike collagen, which is highly allergenic, hyaluronic acid lacks antigenic epitopes [3] [traduction], making it safer as a topical drug matrix. Another advantage of hyaluronic acid is that it can be rapidly degraded by hyaluronidase when adverse events occur [4]. Different molecular weights also influence the biological properties of hyaluronic acid. High-molecular-weight hyaluronic acid has higher viscosity, longer retention time, and better biocompatibility; low-molecular-weight hyaluronic acid exhibits the opposite characteristics [5].
2.2 effets de réparation tissulaire
When inflammation occurs or trauma forms, topically applied high-molecular-weight hyaluronic acid binds with its receptor CD44 to form a hyaluronic acid-CD44 complex, which may trigger a series of reactions in fibroblasts, such as changes in the cellular cytoskeleton and regulation of the tissue healing process [6] [traduction]. During trauma, hyaluronic acid promotes fibroblast migration to the wound site via CD44 expression on fibroblast cells, thereby facilitating tissue healing. However, the receptors of small-molecule hyaluronic acid differ from those of large-molecule hyaluronic acid, and thus this effetis not observed.
Acide hyaluronique à petites moléculesPeut favoriser la phosphorylation de la tyrosine et activer la phospholipase PLCγ1, activant ainsi la voie de transduction du signal de protéine kinase C (PKC) et le système de transduction du signal de protéine kinase activée par mitogène (MAPK), favorisant la mitose des cellules endothéliales vasculaires, favorisant l’angiogenèse et facilitant la réparation des tissus [6].
Komorowicz et al. [7] [traduction] reported that hyaluronic acid with molecular weights of 500 kDa and 1500 kDa caused fibrin to form lateral cross-links rather than branches, thereby altering the fibrin aggregation pattern and inhibiting fibrinolysis; furthermore, on the surface of fibrin clots, 500 kDa and 1500 kDa hyaluronic acid significantly inhibited tissue plasminogen activator (tPA)-catalysed plasminogen activation; therefore, in tissue injury and inflammation, hyaluronic acid can stabilise fibrin by altering its structure and solubility.
2.3. - Effets régulateurs sur l’inflammation
In most studies, high-molecular-weight hyaluronic acid exhibits anti-inflammatory effects when applied topically, while lower-molecular-weight fragments exhibit pro-inflammatory effects. This is primarily due to different receptors on the cellulesurface for hyaluronic acid of different molecular weights, with high-molecular-weight hyaluronic acid primarily binding to CD44 and lower-molecular-weight hyaluronic acid primarily binding to toll-like receptors (TLR) [5].
High-molecular-weight hyaluronic acid binds to CD44 to form a hyaluronic acid-CD44 complex. The signal transduction cascade triggered by CD44 includes PI3K, PDK1, AKT, and the Ras phosphorylation cascade involving RAF1, MEK, and ERK1/2, thereby reducing inflammatory responses and inhibiting the production of reactive oxygen species (ROS). When inflammation occurs, the production of hyaluronic acid synthase increases, leading to enhanced de novo synthesis of small-molecule hyaluronic acid. Concurrently, under the influence of ROS or enzymatic actions such as hyaluronidase, more large-molecule hyaluronic acid is degraded into small-molecule hyaluronic acid. However, simultaneously, CD44 regulates inflammatory responses by downregulating TLR-4 expression. During this process, as large-molecule hyaluronic acid is degraded, ROS are also cleared, exerting an antioxidant effect. Additionally, hyaluronic acid regulates the expression of inflammatory cells, antigen-presenting cells, dendritic cells, and macrophages at the site of inflammation through CD44, exhibiting anti-inflammatory effects [8–11].
In the interaction between small-molecule hyaluronic acid and TLR, TLR-2 and TLR-4 activate NF-κB protein through Myeloid Differentiation Factor 88 (MyD88)-dependent and MyD88-independent pathways, exhibiting pro-inflammatory effects. In the MyD88-independent pathway, hyaluronic acid increases the expression of interferon-induced pro-inflammatory genes through type I interferon [9].
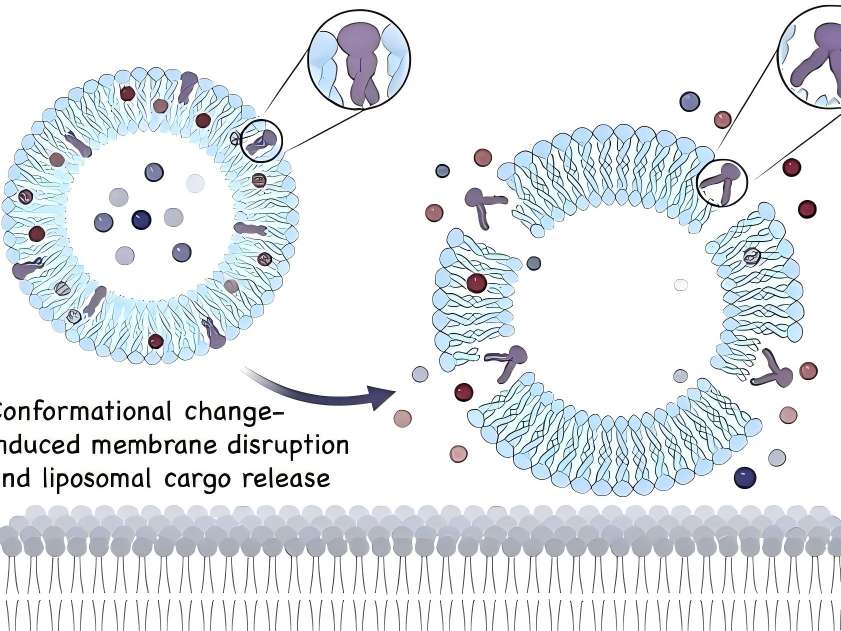
3 Applications cliniques
3.1 systèmes d’administration topique de médicaments
In topical drug formulations for skin diseases, liposomes containing hyaluronic acid are present on the skin surface. Hyaluronic acid can act as a mucosal adhesive agent when the drug takes effect or is absorbed. Additionally, as a topical drug formulation matrix, hyaluronic acid can prolong drug retention time [12].
Friedrichet al. [13] [en] conducted experiments on regulating inflammatory responses associated with acute injury. The combination of high-molecular-weight hyaluronic acid gel with a monoclonal antibody that antagonises TNF-α influenced the bioavailability of the monoclonal antibody, prolonging the drug' S temps d’action au site inflammatoire, augmentant le temps de séjour du médicament, et favorisant ainsi la cicatrisation plus efficacement. Ici, il agit non seulement comme un adhésif muqueux pour aider l’absorption de drogue mais modifie également le drogue' S temps de séjour. Dans un plus grand nombre de médicaments, de tels effets de l’acide hyaluronique peuvent être élucidés davantage.
Un gel de diclofénac 3% avec2.5% high-molecular-weight hyaluronic acid as the matrix (trade name: Solaraze) is increasingly used in the treatment of actinic keratosis. In vitro Franz cell studies showed that compared with the buffer solution control group, after 7 days of treatment with hyaluronic acid formulations, a higher percentage of diclofenac remained in the epidermis (41% vs 25%) [14]. Clinical applications demonstrated good efficacy in clearing skin lesions, with the most common adverse reactions being contact dermatitis, skin dryness, rash, and epidermal peeling; no severe adverse reactions were reported [15].
Advances in nanotechnology have made the application of new technologies possible, such as hyaluronic acid-based nanocapsule polymers, which have shown promising efficacy as a novel topical drug delivery matrix in experimental studies. Compared with non-polymeric micelle solutions containing similar drug concentrations, in vitro skin penetration analysis showed that after 5 hours of local drug application, the drug concentration in the epidermis increased by 3 times, while the drug concentration in the dermis increased by 6 times. Additionally, hyaluronic acid polymer micelles enhanced the drug' S bioactivité [16] [traduction].
3.2 cicatrisation des plaies
Étant donné quehyaluronic acid promotes tissue repair, it can shorten wound healing time and reduce scar formation. Many clinical studies have reported such effects of hyaluronic acid. In the healing of 21 wounds caused by erbium laser, the wounds of subjects treated with oat Rhealba extract and high-molecular-weight hyaluronic acid formulations healed within 9 days, while the control group treated with panthenol and hydroxyproline formulations also healed within 9 days. while those treated with resveratrol copper healed in 12 days, and the untreated control group healed in 16 days. The hyaluronic acid group showed a significant reduction in healing time [17]. In a clinical trial involving 60 cases of local burns (average burn area approximately 3% of body surface area) treated with a high-molecular-weight hyaluronic acid zinc gel, wound size reduced to 50% of the original wound size by day 5, 93.3% of participants achieved complete epithelialisation by day 21, and 91.7% of participants experienced pain relief by day 10. No wound infections occurred during the wound healing process [18].
In a controlled experiment involving 30 cases of second-degree burn healing, olive oil and high-molecular-weight hyaluronic acid had similar effects on burn healing time, but olive oil was more effective in preventing scar formation [19]. In a randomised clinical trial comparing the topical application of high-molecular-weight hyaluronic acid and a neutral medium on 89 cases De jambeveineuxulcers, the results showed that by day 45, the ulcer healing area was significantly larger in the hyaluronic acid group compared to the control group (hyaluronic acid group: 73.4 ± 4.6% vs. control group: 46.9 ± 9.6%, P = 0.011), and the number of healed ulcèresat 45 and 60 days was significantly higher than that in the control group (45 days: hyaluronic acid group 31.1% vs. control group 9.3%, P = 0.011) (60 days: hyaluronic acid group 37.8% vs. control group 16.3%, P = 0.024) [20].
3,3 et 4 Traitement barrière pour la maladie
Studies have shown that impaired epidermal barrier function plays a significant role in the development of atopic dermatitis and other allergic diseases, and dry skin is more prone to eczema. The addition of moisturisers containing hyaluronic acid can improve the integrity of the stratum corneum. Some studies have shown that barrier therapy can reduce the frequency and severity of skin disease flare-ups and decrease the need for topical corticosteroids or topical calcineurin inhibitors. Among these, hyaluronic acid may play a crucial role in the epidermis' Réponse naturelle au traumatisme, y compris la migration des kératinocytes dans la dermatite atopique et la prolifération cellulaire pendant la cicatrisation des plaies et la réparation de la barrière [21].
Palmer et al. [22] conducted a randomised controlled trial to evaluate the efficacy and La sécuritéof MAS063D (a cream containing high-molecular-weight hyaluronic acid) in treating 30 patients with atopic dermatitis. After two weeks of treatment, MAS063D significantly reduced the itch severity index (EASI) in patients; Draelos et al. [23] conducted a controlled trial comparing a 1% high-molecular-weight hyaluronic acid-based pimecrolimus gel with a medicinal ceramide cream in the topical treatment of atopic dermatitis. At the start of the experiment, and at weeks 2 and 4, patients were assessed for erythema, crusting, lichenification, skin peeling, itching, stinging, and burning. At week 2, patients in the hyaluronic acid group showed significant improvement in eczematous lesions compared to the control group, but there was no significant difference in lesion recovery by week 4. Hyaluronic acid-based formulations are easier to apply and absorb than traditional drugs and have a milder odour, improving patient compliance. However, this study had a small sample size, no control group was established, and an appropriate assessment sytigewas lacking, necessitating further experiments to support these results [24].
3.4 maladies inflammatoires
The anti-inflammatory regulatory mechanisms of hyaluronic acid have been demonstrated in some drug delivery media, skin barrier function repair, and wound healing. Additionally, topical hyaluronic acid has shown efficacy in treating facial seborrheic dermatitis. However, in in vitro experiments on inflammation regulation, small-molecule hyaluronic acid often exhibits pro-inflammatory effects (as described in Section 2.3), so the mechanism of topical hyaluronic acid in treating inflammatory diseases remains unclear. The main drugs used for facial seborrheic dermatitis are corticosteroids and antifungal agents, but their application is limited due to adverse reactions and drug sensitivity issues. A clinical trial by Schlesinger et al. [25] showed that topical application of 0.2% sodium hyaluronate improved symptoms such as erythema and itching in patients with facial seborrheic dermatitis. However, this clinical trial had a small sample size, and whether small-molecule hyaluronic acid regulates inflammation in a positive or negative manner remains controversial, so further clinical studies are needed to confirm its efficacy.
4 Conclusion
Topical hyaluronic acid is safe and effective in dermatology. With the maturation of bacterial fermentation methods for Production d’acide hyaluronique, sa biosécurité a été encore améliorée et les coûts de production ont diminué par rapport aux méthodes précédentes. Cela le rend plus approprié pour des applications topiques. Avec le développement continu de la biotechnologie, l’émergence de nouveaux matériaux tels que les nano-particules polymères micelles pourrait permettre à l’acide hyaluronique de présenter de meilleures propriétés physico-chimiques pour une utilisation topique en dermatologie.
In many skin lesions, such as psoriasis, the normal hyaluronic acid reticular structure is partially missing in the spinous layer and granular layer, and hyaluronic acid is present in the stratum corneum of dyskeratosis. Whether correcting the abnormal distribution of hyaluronic acid in the epidermis of psoriasis patients can improve the symptoms of related skin diseases is worthy of further study. Studies have shown that with the increase of age, the expression of hyaluronic acid and CD44 receptor in the skin showed a downward trend. At this time, the role of exogenous hyaluronic acid in various aspects was weakened, so whether there were differences in the dosage and frequency of use at different ages is still worth discussing. Because hyaluronic acid exerts its antioxidant effect through its own degradation and ROS elimination mechanism, its application in anti-aging drugs is worth tracking.
Référence:
[1] Liang J,Jiang D,Noble PW. Hyaluronan as a thérapeutique Cible en humain Maladies [J]. Adv: La drogue délivre Rev,2016, 97:186-203.
[2]Stern R,Asari AA,Sugahara KN. Fragments de Hyaluronan: un système riche en informations [J]. Eur J Cell Biol,2006,85 (8) : 699-715.
[3] À propos de Nowacki L,Pietkun K, pokrywczy[unused_word0002] ska M,et al.Filling effets, persistance,et safety De la peau Produits de comblement Formulé avec stem cellules Dans un modèle animal [J]. Aesthet Surg J, 2014,34(8) : 1261-1269.
[4]DeLorenzi c.dégradation transartérielle du remplissage d’acide hyaluronique par l’hyaluronidase [J]. Dermatol Surg,2014,40(8) : 832- 841.
[5]Zhao N,Wang X,Qin L,et al.effet du poids moléculaire Et concentration de l’hyaluronansur la prolifération cellulaire et la différenciation osseogène in Vitro [J]. Accueil» Biochem Les Biophys fr Commun,2015,465(3) : 569-574.
[6] Slevin M,Kumar S,Gaffney j.oligosaccharides angiogéniques of hyaluronan induire multiples signalisation Les voies d’accès affectant Cellules endothéliales vasculaires mitogènes et cicatrisation des plaies respon- ses[J]. J Biol Chem,2002,277(43) : 41046-41059.
[7] Komorowicz E, bal
[8]Petrey AC,de la Motte CA.Hyaluronan, un régulateur crucial de l’inflammation [J]. Front Immunol,2014,5:101.
[9]Naor D.Editorial: Interaction entre l’acide hyaluronique et ses récepteurs (CD44,RHAMM) réglemente the Activité: D’inflammation et de Cancer[J]. Front Immunol,2016,7:39.
[10]Vigetti D,Karousou E,Viola M,et Al.Hyaluronan: bio- synthèse et signalisation [J]. Biochim Biophys Acta,2014, 1840(8) : 2452-2459.
[11] [traduction] Kim Y,Lee YS,Hahn JH,et al.cibles d’acide hyaluronique CD44 et inhibe la signalisation FcepsilonRI impliquant PKCdel- ta,Rac1,ROS, et Plan du site to exercer anti-allergique effect [J]. Mol Immunol,2008,45(9) : 2537-2547.
[12]Law CH,Li JM,Chou HC,et al. Protection des données in H9C2 Cardiomyocytes: a cell modèle De la blessure d’ischémie-reperfusion cardiaque et du traitement [J]. Toxi- cology,2013,303:54-71.
[13] Friedrich EE,Washburn N ° transports modèles of Anti - Tnf-α dans les brûlures: implications thérapeutiques de l’hyalu - Conjugaison acide ronique [J]. Biomaterials,2017,114:10-22.
[14]Brown MB,Hanpanitcharoen M,Martin GP. Etude in vitro de l’effet des glycosaminoglycanes sur la peau Partitionnement et dépôt of NSAIDs[J]. J J J J J J Pharm, 2001,225(1-2) : 113-121.
[15]Gupta AK,Paquet M,Villanueva E,et al. Kératoses actiniques [J]. Cochrane (en anglais) Base de données Système Syst Rev,2012, 12.
[16] Mejkalolio-d,Muthn∮ T, neporolio-k,et al.Hyaluronan polymères micelles pour l’administration topique de médicaments [J]. Carbohydr Polym,2017,156:86-96.
[17]Sabadotto M,Theunis J,Black D,et al. Évaluation in vivo de l’effet d’une crème contenant de l’avena Rhealba( ) extrait et acide hyaluronique sur la restauration de la peau Laser [J]. Eur J Dermatol,2014,24(5) : 583-588.
[18] juhlcpe z I, zoltlcpe P,Erdei i.traitement des brûlures d’épaisseur partielle au Zn-hyaluronan: leçons d’une étude pilote clinique [J]. Ann Burns Fire Disasters,2012,25(2) : 82-85.
[19]Campanati A,De Blasio S,Giuliano A,et al.huile ozonée topique contre gel hyaluronique pour le traitement des Pleine épaisseur Deuxième degré Brûlures: A Prospective, comparative, à aveugle unique,non randomisée, clinique contrôlée Trial [J].Burns,2013,39(6) : 1178-1183.
[20]Humbert P,Mikosinki J,Benchikhi H,et al.efficacité et Innocuité d’un tamis de gaze contenant de l’acide hyaluronique dans le traitement of leg ulcers of venous or Origine mixte: a Double aveugle, Randomisé, contrôlé Procès [J]. Int Int blessure J,2013,10 (2) : 159-166.
[21]Maytin EV,Chung HH,Seetharaman VM. L’hyaluronan participe à la réponse épidermique à la perturbation de la barrière de perméabilité in vivo[J]. Am J Pathol,2004,165 (4) : 1331 — 1341. [22]Palmer CN,Irvine AD,Terron-Kwiatkowski A,et al.Com- Mes Variantes de perte de fonction de la protection de barrière épidermique de tein filaggrin sont un facteur prédisposant majeur pour la der- matite atopique [J]. Nat Genet,2006,38(4) : 441-446.
[23]Draelos ZD. Une évaluation clinique de l’efficacité comparable De mousse à base d’acide hyaluronique et de crème d’E - mulsion contenant du céramide dans le traitement d’atopiques légers à modérés Dermatite [J]. J Cosmet Dermatol,2011,10(3) : 185-188.
[24]Frankel A,Sohn A,Patel RV,et al.étude de comparaison bilatérale de la crème de pimécrolimus 1% et d’une mousse émolliente à l’acide céramide-hyaluronique dans le traitement de patients atteints de dermatite atopique [J]. J Drugs Dermatol,2011,10(6) : 666-672.
[25]Schlesinger T,Rowland PC. Efficacité et sécurité d’un gel topique d’acide hyaluronique de faible poids moléculaire dans le traitement de la dermatite séborrhéique du visage rapport final [J]. J J J Clin Aesthet Dermatol,2014,7(5) : 15-18.
-
Précédent précédent
Quelle est l’utilisation de l’acide hyaluronique sur les produits de soin du visage?
-
Suivant:
Quelle est l’utilisation de l’acide hyaluronique dans le domaine Oral?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




