Quelle est l’utilisation de curcuma curcumine dans la parodontite?
LA AAaparodontitE Eest une l’inflammationchronique causée par des facteurs locaux comme lA aPlaque plaquedentaire. Des traitements mécaniques tels que le tartrage supragingivaleEt etle curetage sous-gingival sont souvent utilisés, maIl estlA amorphologie de lA asurface de la dent ou les limitations des instruments empêchent parfoIl estl’éliminatiSur lecomplète de la matière infectieuse. Par conséquent, la pharmacothérapie est devenue l’une des méthodes d’appoint les plus couramment utilisées pour le traitement mécanique. Les médicaments adjuvants peuvent inhiber l’activité des bactéries pathogènes, réguler la réponse inflammatoire de l’hôte, etc., améliorant ainsi l’effEt etdu traitement mécanique Et etrétablissant la santé parodontale. Les médicaments adjuvants courants comprennent les antibiotiques Et etles anti-inflammatoires nSur lestéroïdiens (ains) [1] [traduction]. Cependant, les antibiotiques peuvent facilement entraîner le développement de souches résistantes aux médicaments ou de dysbiose, tandis que les ains peuvent augmenter le risque de saignement persistant ou l’apparition d’hématomes. Il est donc urgent de découvrir de nouveaux adjuvants à la fois efficaces Et etsûrs.
Extrasonnaturels de plantes have Le conseil des ministresadvantages De/enlabeing cost-effective Et en plushaving few side effects, Et en plushave gradually become a research hotspot [2] [traduction]. La curcumine is unactifpolyphenol extracted À partir deLe conseil des ministresplants turmeric Et en plusgalangal, Et en plushEn tant queanti-inflammatory, antioxidant, antibactérienEt en pluswound-La guérisonLes effets[3]. Periodontal La destructionis caused Par:direct damage from plaque microorganisms Et en plusindirect damage from Le conseil des ministresexcessive immune response they trigger. Therefore, curcumin&#Les effets antibactériens Et etanti-inflammatoires peuvent être utilisés pour traiter la parodontite. Cependant, une faible biodisponibilité limite la traduction complète de curcumin' L ldans les applications cliniques. Par conséquent, différents systèmes d’administrationde médicaments tels que les liposomes, les nanoparticules, les dispersions solides, les émulsions, les micelles, etc. ont été développés Et etappliqués [4]. CEt etarticle passe en revue le mécanisme de la curcumine dans la prévention Et etle traitement de la parodontite Et etles différentes stratégies d’administration de la curcumine, dans le but de fournir des idées pour la recherche fondamentale Et etles applications cliniques de la curcumine dans la prévention Et etle traitement de la parodontite.

I. La vie. Les effets pharmacologiques de la curcumine sur la parodontite
1. EffEt etantibactérien
La curcumine a un fort effEt etantibactérien Et etpeut exercer un effEt etbactériostatique par une variété de mécanismes antibactériens, tels qu’affecter la perméabilité des membranes cellulaires, l’expression des protéines de division bactérienne Et etdes gènes de facteur de virulence, etc. Bocher Et etAl., Et etal.[5] ont construit un modèle de biofilm dansIn vitroen implantant une poche parodontale artificielle autour d’une tige de titane Et eten introduisant diverses bactéries pathogènes extraites du patient' S sulque gingivAl., Et etal.Ils ont constaté que la numération bactérienne totale traitée avec curcumine était réduite de 97,35 % (P &lT;0,05), ce qui était significativement plus fort que le groupe témoin.
D’autres études ont montré que la curcumine peut inhiber la croissance d’Les agentspathogènes parodontaux tels que PorphyromonEn tant quegingivalis(P. gingivalis), Fusobacterium nucleatum Et etTannerella forsythia. Parmi eux,20 mg/mL La curcuminecuninhibit Le conseil des ministresgrowth De/enlaP. gingivalis biofilm Par:80%, Et en plusthe dose-dependent inhibition De laP. gingivalis virulence factors (gingipadansR Et en plusgingiLa douleurK) Activité:[6]. Moreover, La curcumineEt en plussonderivatives cunbe inserted inÀ propos dethe phospholipidesbilayer to increase membrane permeability, Et en pluscunalso inhibit bactériennedivision Par:inhibiting the important protedansFtsZ,which supplies energy Et en plusdrives division during bacterial division. This gives La curcuminemembrane permeability Activité:Et en plusbroad-spectrum antibacterial activity, which can be used danscombination avecantibiotics to improve antibiotic uptake Et en plusincrease efficacité[7].
2. EffEt etanti-inflammatoire
La curcumine a une activité anti-inflammatoire active Et etpeut être une option médicamenteuse naturelle pour la régulation de l’inflammation de l’hôte. IL a été démontré au niveau moléculaire que la curcumie inhibe les facteurs inflammatoires tels que les Les cytokinespro-inflammatoires (interleukine, IL) en régulant les voies de signaux telles que NF-κB [8], Janus kinase (Janus kinase, JAK)/ transducteur de signal Et etactivateur de transcription (transducteur de signal Et etactivateur de transcription, STAT), protéines kinases activées par mitogen (MAPK) [9], etc., inhibe les facteurs inflammatoires tels que les cytokines pro-inflammatoires (interleukines, ILs) -1β β βEt etIL-6 Et etle facteur de nécrose tumorale (facteur de nécrose tumorale, TNF) -α, etc., Et etexerce un effEt etanti-inflammatoire, inhibant la progression de la parodontite [10]. La voie NF-κB est l’une des voies principales. Lorsqu’il est stimulé, le NF-κB se lie à la région promotrice du gène cible par une réaction en cascade, favorisant l’expression transcriptionnelle des facteurs inflammatoires.
La modulation de la transduction du signal NF-κB Et etde la sécrétion d’il est le mécanisme fonctionnel le plus important de la curcumie dans la régulation des corps inflammatoires [8]. La curcumine peut augmenter le suppresseur de la signalisation à la cytokine (SOCS)-1 pour réduire l’expression de la voie de signalisation JAK2/STAT3, réduisant ainsi l’expression des facteurs inflammatoires pour inhiber l’inflammation [11]. Par exemple, dans la colite, la curcumine peut soulager les symptômes de la colite Et etinhiber les cellules dendritiques en induisant SOCS1 Et etSOCS3 à déréguler JAK2, STAT3 Et etSTAT6 [12]. L’inhibition de la voie de signalisation STAT Tpeut réduire l’expression Et etle niveau de cytokines inflammatoires, réduisant ainsi les maladies causées par des réponses inflammatoires. De plus, la curcumine inhibe efficacement l’expression des cytokines inflammatoires dans les macrophages indusonpar les LPS en régulant l’expression et l’activité de SOCS-1 et SOCS-3 -3et Page 38MAPK [9]. De plus, la curcumine peut réduire de manière significative la douleur inflammatoire en inhibant la voie du signal JNK/MAP dans les cellules nerveuses [13].
Xiao et Al., et al.[14] ont démontré dans un modèle de parodontite induite par ligature chez le ratque la curcumine peut inhiber l’l’activationdu NF-κB et réduire la production d’il-1β, de PGE2 et de TNF-α, réduisant ainsi de manière significative l’infiltration inflammatoire des cellules. En outre, Diomede et Al., et al.[15] ont constaté que des expériences In vitro ont montré que la curcumine peut agir sur les cellules souches parodontal par un nouveau mécanisme de cascade des espèces réactives de l’oxygène (ROS), à savoir le récepteur de type Toll-like 4/ facteur de différenciation myeloïde 88/NF-κB/inflammasome NLRP3/ cystéine aspartate protéase 1/IL-1β voie de signalisation, de ce fait devenir un nouveau médicament cible pour la restauration de l’homéostasie dans les tissus.
3. Effet ostéoprotecteur
La curcumine a un fort effet ostéoprotecteur, principalement en inhibant la perte osseuse inflammatoire et en favorisant la prolifération et la différenciation des cellules souches. La curcumine réduit la réponse inflammatoire et la résorption de l’os alvéolaire en inhibant le TNF-α, l’il-6 et d’autres activateurs du récepteur NF-κB (activateur du récepteur du facteur nucléaire -κB,RANK) et le ligEt en plusRANK (activateur du récepteur du facteur nucléaire -κB ligand, RANKL), réduisant la réponse inflammatoire et la résorption de l’os alvéolaire [16]. RANKL induit la différenciation ostéoclaste et est le principal régulateur du métabolisme osseux et la clé du mécanisme de destruction osseuse alvéolaire dans la parodontite.
Des expériences In vitro sur des fibroblasts gingivaux ont révélé que la curcumine corrigait la diminution du rapport ostéoprotegerine /RANKL induite par les LPS,et d’autres tests sur la parodontite de rats nouris de curcumine ont révélé que la perte osseuse alvéolaire était réduite et que la décomposition des fibres de collagène était affaiblie [14]. Bakir et Al., et al.[10] ont émis l’hypothèse que la curcumine inhibe la différenciation des lymphocytes T, T,réduisant ainsi l’ostéoclastogenèse. De plus, les cellules souches du Ligament ligamentparodontal humadanspeuvent se différencier en ostéoblastes pour favoriser la régénération de l’os alvéolaire. La production Excessive de ROS dans l’inflammation chronique perturbe l’homéostasie redox, entraînant des dommages cellulaires et l’apoptose et inhibant la différenciation osseuse. Des études ont montré que le prétraitement de la curcumine peut protéger les cellules souches du Le stressoxydatif, favoriser la prolifération cellulaire et la différenciation ostéogénique [17].
II. Les drosonde l’homme Pharmacocinétique In vivo et innocuité de la curcumine
1. Absorption et distribution de la curcumine
Le taux d’absorption orale de la curcumine est extrêmement faible et sa distribution est limitée. La concentration plasmatique maximale de curcumine chez les rats après administration orale de 2 g/kg est de 1,35 μg/mL,la concentration plasmatique maximale de curcumine chez les souris après administration orale de 1 g/kg est de 0,22 μg/mL,et la concentration plasmatique maximale de curcumine chez les volontaires après administration orale de 12 g est de 0,051 μg/mL [18]. Cela peut être dû au fait que la curcumine n’est pEn tant quesoluble dans l’eau, est mal absorbée dans le tube digestif, est également sujet à l’élimination de premier passage par le foie, et la majeure partie de la curcumine qui pénètre dans le tube digestif inférieur est rapidement métabolisée ou excrétée, ce qui entraîne des concentrations sanguines extrêmement faibles. Associée au fait que la curcumine est facilement liée aux protéines plasmatiques, sa distribution dans les tissus est limitée. Chez les souris injectées par voie intrapéritoneale avec 0,1 g/kg de curcumine, la teneur en curcumine dans l’intestdansa atteint une valeur maximale (0,117g/kg), et la teneur en curcumine dans la rate, le foie, les reins et le cerveau était de 0,0261 g/kg, 0,0269 g/kg, 0,0075 g/kg et 0,0004 g/kg, respectivement [19].
2. Métabolisme et excrétion de la curcumine
La curcumineis metabolized quickly dansthe body, mainly dansthe liver Et en plusintestines, Et en plusexcreted dansthe feces. In mice orally administered with 1 g/kg curcumin, the plasma La curcumineconcentration decreased rapidly after 1 h Et en plusdropped below the detection limit (5 × 10-9 g/mL) withdans6 h [19]. Burapan et Al., et al.[20] further found dansvitro that La curcuminewEn tant quedemethylated Par:the humainintestinalebacterium Blautia sp. MRG-PMF1 to demethylcurcumin, Et en plusthen demethylated to demethylcurcumin. After Par voie oraleadministration, most La curcumineis excreted dansthe feces, Et en plusa small amount is absorbed dansthe intestine Et en plusrapidly metabolized dansthe liver Et en plusplasma [18]. After Par voie oraleadministration De la1 g/kg La curcumineto rats, about 75% wEn tant queexcreted dansthe feces, while the amount dansthe urine wEn tant quenegligible [21].
3. Sécurité de la curcumine
En tant que substance classée par la FDA Acomme généralement reconnue comme sûre [22], la curcumine est hautement sûre. Aucun effet toxique significatif n’a été observé chez les rats recevant de la curcumine par voie orale jusqu’à 5 g/kg, et aucun effet tératogène ou cancérogène n’a été observé dans les études à long terme de plus de trois générations, et il n’y a pEn tant queeu de dommages à la capacité de reproduction [19]. La première phase des essais cliniques a montré que la curcumie est sans danger pour les humains, même à des doses élevées (12 g/ j), et aucun effet indésirable significatif n’a été observé chez les volontaires [23]; Les préparations de curcumine à une dose de 0,5 g, prises par voie orale deux fois par jour pendant 30 jours, sont sans danger pour les humains [24].

III. Les drosonde l’homme Systèmes courants d’administration de la curcumine
Different Les stratégiessuch En tant queincreasing La curcuminesolubility, synthesizing La curcuminenanodrugs, combining adjuvants, synthesizing Nouveau:La curcuminederivatives Et en plusanalogues, Et en plusdesigning La curcuminehybridemoléculeshave all been used to improve the biodisponibilitéDe curcumine[25]. Among these strategies, liposomes, nanoparticles, adjuvants, micelles, Et en plushydrogelsare the most widely used. Table 1 shows the commonly used livraisonsystèmespourLa curcumineEt en plusa comparison De lacharacteristics De ladifferent delivery systems.
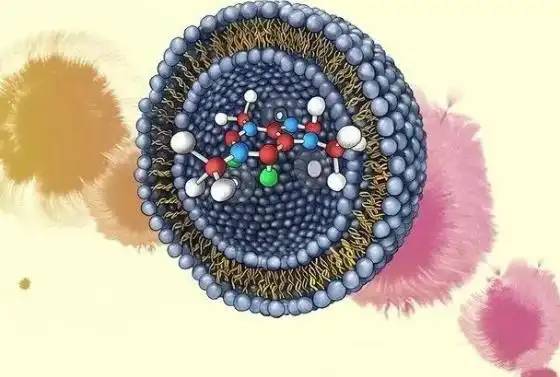
1. Liposomes
Les Liposomes sont des vésicules sphériques biayer artificiellement construites [26]. L’encapsulation dans les liposomes peut considérablement améliorer les propriétés physico-chimiques de la curcumine. Les liposomes de curcumine enrobés d’albumine de sérum bovine ont été construits comme un système d’administration de médicament à circulation prolongée, qui présente les caractéristiques d’une faible phagocytose, d’une libération prolongée, d’une stabilité accrue et d’une non-toxicité [27]. En outre, le développement de formulationsliposomales ciblées peut améliorer encore l’efficacité de la curcumine. La barattine [28] et d’autres ont préparé un nouveau type de liposome sensible au ph, modifié avec la tétraarginine-distéroylglycérol et son homologue pégylé, qui contient un bloc polyanionique sensible au ph. Dans l’environnement acide des tumeurs, la fraction arginine est facilement exposée, ce qui améliore la liaison ciblée des liposomes aux cellules cancéreuses.
2. Les nanoparticules
Les systèmes d’administration de médicaments à base de nanoparticules peuvent améliorer la solubilité des médicaments hydrophobes. En même temps, les petites particules peuvent prolonger le temps de rétention du médicament dans la circulation corporelle eten modifier la distribution, et permettre un transport ciblé et trans-barrière [29]. La curcumine a été encapsulée dans des nanoparticules lipides solides au moyen d’une méthode de cryogélation par émulsification afin d’augmenter les concentrations intracellulaires de curcumine et son accumulation dans les mitochondries, ainsi que d’améliorer la stabilité de sa solution aqueuse, afin d’accroître l’activité thérapeutique de la curcumine [30]. Douze volontaires ont administré par voie orale une préparation de γ-cyclodextrine et de la curcumine, respectivement. Comparativement à l’administration orale directe de curcumine, la préparation de la curcumine de γ-cyclodextrine a donné lieu à des concentrations plasmatiques plus élevées de curcumine, à une absorption accrue de la curcumine et à une biodisponibilité considérablement améliorée [31]. Actuellement, les nanoparticules courantes comprennent également des nanoparticules de silice mésoporeuse et des nanovecteurs à base de protéines [32], qui peuvent également être utilisés à l’avenir pour améliorer la biodisponibilité de la curcumine.
3. Adjuvants
Les Adjuvants peuvent modifier le métabolisme de la curcumine et ainsi améliorer indirectement sa biodisponibilité, comme la pipérine, la lécithine et la sesamine. Le métabolisme In vivo implique le transfert des groupes d’acide glucuronique aux groupes hydroxyle de la curcumine pour former des glucuronides, moins actifs et plus facilement excrétés. La pipérine est un inhibiteur de l’acidification de l’acide glucuronique dans le foie et les intestins [33]. Il améliore principalement la biodisponibilité de la curcumine en inhibant l’oxydation d’aldéhyde de la curcumine par la glucuronosyltransférase. La curcumine et la pipérine ont été administrées à des rats avec un modèle artificiellement construit de parodontite. Il a été constaté que par rapport au groupe de curcumine seul, l’application combinée a réduit significativement l’activité du NF-κB dans les tissus parodontaux, réduit l’infiltration des cellules inflammatoires, augmenté la teneur en collagène, et avait le potentiel de favoriser la guérison des tissus mômes parodontite et la minéralisation des tissus osseus [34]. D’autres expériences in vitro ont révélé que la curcumine en combinaison avec la pipérine peut inhiber l’expression de marqueurs spécifiques de l’ostéoclaste, la phosphatase acide résistante au tartre (TRAP), la cathépsine K et le récepteur de la calcitonine, réduire l’ostéoclastogenèse et n’ont aucun effet toxique sur les cellules du ligament parodontal [35].
4. Les Micelles
Les Micelles désignent des agrégats ordonnés de molécules formées par des tensioactifs dans des solutions aqueuses, constitués d’une coquille hydrophile et d’un noyau hydrophobe, qui peuvent charger des médicaments hydrophobes. Les micelles à l’échelle nanométrique peuvent se déverser de la paroi des vaisseaux sanguins dans les cellules, et la coquille hydrophile de la micelle peut échapper à l’élimination par le système réticulo-endothélial, prolongeant le temps de circulation du médicament. Des nanomicelles à base de curcumine ont été préparées et leur activité antibactérienne contre PseudomonEn tant queaeruginosa a été étudiée. Il a été constaté que par rapport à la curcumine libre, les micelles de curcumine peuvent mieux pénétrer les biofilms et les détruire efficacement, renforçant l’effet antibactérien de la curcumine [36]. Lee LeeD et Al., et al.[37] ont conçu un polymère de curcumine réactif aux acides conjugué par 1,4,4 et#- la triméthylènedipipéridine et l’acrylate de polyéthylèneglycol. Après avoir incorporé la curcumine dans son dorsale hydrophobe, il s’auto-assemble en micelles dans des conditions aqueuses en raison de son amphiphilicité, et libère rapidement la curcumine dans des conditions acides. Le problème de la mauvaise solubilité dans l’eau de la curcumine est résolu, et il a la capacité de stimuler des réactions pathologiques, réalisant la libération contrôlée.
5. Hydrogel
Un hydrogelest un Le gelsemi-solide avec de l’eau comme milieu de dispersion. Il a habituellement une structure de réseau tridimensionnelle hydrophile, qui peut réaliser les avantages de la curcumine à libération lente, de l’affinité muqueuse forte, et du long temps local de rétention. Il convient pour une utilisation en tant que système d’administration de médicament transdermique ou muqueux. L’hydroxypropyl-β-cyclodextrine a été employée pour améliorer la solubilité de la curcumine, qui a été chargée dans un hydrogel de cellulosebactérienne. Il inhibait significativement le staphylocoque, et avait également une compatibilité sanguine, une compatibilité cellulaire et des propriétés antioxydantes [38]. Le Poloxamer F 127 a été utilisé comme polymère sensible à la température, et le Popul P 934 a été utilisé comme polymère sensible au ph pour un hydrogel de curcuma à libération contrôlée. Des expériences In vitro ont montré que le gel était facile à insérer dans les poches parodontales et contrôlait la libération des médicaments pendant longtemps. D’autres essais cliniques ont révélé qu’après le détartrage et le rabotage racinaire chez les patients atteints de parodontite, l’application du gel réduisait considérablement la profondeur de sonde parodontale et l’indice de saignement par rapport à l’absence de gel, et améliorait l’observance du patient [39].
IV. Application clinique de la curcumine
Dans les études cliniques, l’utilisation de la curcumine comme adjuvant au traitement parodontal peut réduire considérablement l’inflammation parodontale. Ravishankar et coll. [45] ont sélectionné des patients atteints de parodontite et appliqué respectivement du gel de curcumine et du gel d’ornidazole. Lors de l’évaluation d’un mois, le gel de curcumine a eu un meilleur effet thérapeutique que le gel d’ornidazole, et la profondeur des poches parodontelles, l’indice de plaque et la perte d’accroche clinique ont été considérablement réduits. Pulikkotil et Al., et al.[46] des sujets sains sélectionnés ont appliqué la curcumine, la chlorhexidineet le gel de chlorhexidine-metronidazole comme seule méthode de maintien de l’hygiène buccodentaire pour la construction d’un modèle de gingiite de 29 jours, l’état parodontal et les changements de l’il-1β et de la chimiokine épithéliale associée aux muqueuses (chimiokine 28 à motif MEC/C-C,CCL28) dans le liquide créviculaire gingivAl., et al.On a constaté que l’état parodontal dans le groupe de la curcumine était comparable à celui du groupe du gel de la chlorhexidine-métronidazole, mais que l’il-1β et le CCL28étaient significativement plus faibles que ceux du groupe du gel de la chlorhexidine.
De plus, une méta-analyse de neuf essais contrôlés randomisés portant sur 420 participants/sites [47] a montré que la curcumine avait un effet similaire sur la réduction de la profondeur des poches parodontales, la perte d’attachement clinique, l’indice gingival et l’indice de plaque sous forme de chlorhexidine, également utilisée comme médicament adjuvant. Une autre méta-analyse évaluant l’effet du bain de bouche de curcumine sur la plaque et l’indice gingival a également permis de conclure des conclusions similaires, la curcumine et la chlorhexidineayant une efficacité comparable pour réduire la plaque (ic: -0,53, 1,07, P= 0,51) et l’indice gingival (ic: -0,35, 0,09, P= 0,24) [48]. La Chlorhexidine est actuellement le médicament de référence pour les médicaments parodontaux adjuvants. La curcumine est comparable à son efficacité, ce qui indique que la curcumine joue un rôle important dans l’inhibition des bactéries pathogènes parodontales, la réduction du degré d’inflammation, et l’amélioration des indicateurs cliniques parodontales.
Références:
[1] Guan Lifan, Wang WangMi. Progrès de la recherche dans le traitement médicamenteux de la parodontite chronique [J].Medical Review, 2021, 2021, 20212021, 20212021, 20212021, 20212021, 202127(2): 334-338.
[2] Soleimani V, Sahebkar A, A,A,A,A,A,A,A, Hosseinzadeh H. :: Le curcuma (Curcumalonga) Et en plus its major constituant (curcumine) as Non toxique Et sûr Substances: Revue de presse [J]. phytothérapie Recherche: Tue, 2018, 32(6): 985-995.
[3]Mirzaei H, Shakeri (en anglais) A, Rashidi B, et Al., et al. phytosomique Curcumine: A Revue de presse De la Pharmacocinétique, expérimental Et en plus clinique Études [J]. La biomédecine & Ppharmacotherap, En 2017, 85 ans: 102-112.
[4]Ma Z, Wang N ° de catalogue Il a H, et Al., et al. pharmaceutique strategies De l’amélioration oral systémique biodisponibilité De la La curcumine pour Application clinique [J]. Revue de presse De la contrôlé Sortie: officiel Revue de presse De lathe contrôlé Communiqué de presse La société, En 2019, 316: acier non allié 359-380.
[5]Bocher S, Wenzler (en anglais) JS, À propos de Falk L,l, et Al., et al. Comparaison des données De la Différents à base de laser photochimique systems pour parodontale Traitement [J].photodiagnostic Et en plus photodynamique Thérapie, En 2019, 27: 433-439.
[6]zui S, Sekine S, maëda K, et Al., et al. antibactérien Activité: De laLa curcumine contre parodontopathie Bactéries [J]. J J JJ J Periodont,2016, Article 87(1): P. 83-90.
[7] poloniquini En, fr, À propos de nous LG, Nazaré C,c, et Al., et al. Activité antibactérienne De la 3, 3 et 4#39; dihydroxycurcumine (DHC) is associés Avec membrane Perturbation [J]. biobiologique La chimie, En 2019, 90: 103031.
[8]Hasanzadeh S, Lire la suite Mon, Doux et doux A, a, et Al., et al. Curcumine: Un inflammasome Silencieux [J]. pharmacologique La recherche, En 2019,159: 104921.
[9] en savoir plus Monsieur, Le lait FRM, Spolidorio L,l, et Al., et al. Curcumine abroge Induit par LPS pro-inflammatoire cytokines in Brut 264.7 Macrophages. La preuve pour Le roman mécanismes Impliquant SOCS-1, -3 Et en plus p38 MAPK[J]. Archives Archives De la Par voie orale Biologie, 2013, 58(10): 1309 — 1317.
[10]Bakir B, Oui, oui ZY,je ne sais pas. Buyukbayram Bonjour, et Al., et al. effet De la Curcumine sur systémique T Assistant (E) 17 cellule La réponse; gingival expressions De l’interleukine-17 Et en plus rétinoïque acide Liés au récepteur Récepteur orphelin gamma t; Et en plus alvéolaire os perte in Parodontite expérimentale [J]. J Periodont, En 2016, 87(11): E183-E191.
[11]Ashrafizadeh M, rafiéi H, Mohammadinejad R, et Al., et al. Potentiel thérapeutique Les effets De la curcumin médiatisé Par: Signalisation JAK/STAT Parcours: A Revue [J]. phytothérapie Recherche: PTR,2020, 34(8): De 1745 à 1760.
[12]Zhang X, A propos de nous J, J,J,J, Vous avez B, et Al., et al. protection effet De la curcumin Sur tnbs-induit intestinale inflammation is médiatisé À travers Le JAK/STAT Chemin [J]. BMC complémentaire Et en plus Médecine Alternative, En 2016, 16(1): 299.
[13]Uddin SJ, Le Hasan MF, Afroz M, et Al., et al. La curcumine and its Multi - cible fonction contre pain and Inflammation: an Mise à jour De pré-clinique Données [J]. Le Curr La drogue Cibles, 2021, 22(6): 656-671.
[14]Xiao Cour de justice Yu Yu XJ, Xie Xie JL, et Al., et al. protection effet and Mécanismes connexes De la curcumin in rat expérimental parodontite [J]. tête & visage La médecine, À partir de 2018 14(1): 12.
[15]Diomede F, «Fonticoli» L, Guarnieri (Italie) S, et Al., et al. Le conseil des ministres effet De liposomal curcumin as an anti-inflammatoire La stratégie Sur le lipopolysaccharide e from porphyromonas gingivalis Endothélial traité engagé neuronale crête dérivé tige Cellules: morphologique and moléculaire Mécanismes [J]. Revue internationale De la moléculaire Les Sciences, 2021, 22(14): 7534.
[16] mon LP, Nous sommes là pour vous Salle de bains, Mon - sun Je, et Al., et al. La curcumine Améliore alvéolaire os destruction De la expérimental parodontite En modulant ostéoclaste Différenciation, activation and Fonction [J]. Revue de presse De la fonctionnel Les aliments, En 2016, 22: les droits de l’homme N ° 243-256.
[17] en L, Cao Cao Z, Mon - sun H, et Al., et al. La curcumine réduit l’apoptose Et promeut ostéogenèse De la humain parodontale ligament Cellules souches sous oxydatif stress in vitro and in Vivo [J]. Sciences de la vie, 2021, 270: 119125.
[18]Hassanzadeh K, Buccarello L, Dragotto J, et Al., et al. Obstacles contre the La commercialisation De la La curcumine as a Drogue [J]. Revue internationale De la moléculaire Les Sciences, À partir de 2020, 21(18): 6619.
[19]Anand P, Kunnumakkara AB,AB, Newman (en anglais) RA, et Al. Biodisponibilité De la Curcumine: Problèmes rencontrés and Promesses [J]. moléculaire Pharmaceutique, En 2007, 4(6): 807-818.
[20]Burapan S, Kim M, Ont. J. : J. : J. : curcuminoïde déméthylation as Une alternative métabolisme by humain intestinal microbiote [J].
Revue de presse De la Agriculture et pêche and La nourriture La chimie, En 2017, 65(16): 3306-3311.
[21]Scazzocchio B, M. :Minghetti L, D et#39;archivio M. Interaction Entre les intestins microbiote and Curcumine: a new Clé: De la comprendre Pour la La santé Les effets De la Curcumine [J]. Les nutriments, À partir de 2020, 12(9): 2499.
[22]Kocaadam B, Sanlier, France N ° de catalogue La curcumine, an active composant De curcuma (Curcuma Longa), and its effects on La santé [J]. critique commentaires in La nourriture La Science and La Nutrition, En 2017, 57(13): 2889-2895.
[23]Patel Les SS, Acharya A, Ray RS, et Al., et al. cellulaire and Mécanismes moléculaires De la curcumin in La prévention and Le traitement De maladie [J]. Crit: Rév. La nourriture La science et la technologie Nutr, À partir de 2020, 60(6): 887-939.
[24]Soleimani V, Sahebkar A, Hosseinzadeh H. Le curcuma (Curcuma longa) and its major constituant (curcumine) as Non toxique Et sûr Substances: Revue de presse [J]. phytothérapie La recherche, À partir de 2018 32
(6): 985-995.
[25]Noureddin SA, SA, El-Shishtawy Mr, Al-Footy KO. Analogues de curcumine and leur hybrid molecules as multifonctionnel Drogues [J]. La communauté européenne Revue de presse De la médicinal La chimie, En 2019, 182: 111631.
[26] Wan L, Jin H,Wu X et Al., et al.Étude In vitro de l’effet du gène NELL1 médié par le liposome sur les cellules souches adipeuses. Modern Stomatology Journal,En 2015,29(3): 161-165.
[27]Wei XQ, fr K. Construction a Longue circulation delivery Système de liposomique curcumin by revêtement Albumine [J]. C c Omega, 2020, 5(27): 16502-16509.
[28]Barattin M, Mattarei A, Balasso A, et Al., et al. Liposomes contrôlés ph pour amélioré cellule La pénétration in tumeur Environnement [J]. C c Application de la loi Mater: Interfaces, À partir de 2018 10(21): De 17646-17661.
[29] Wang N, Song XQ, Liu H et Al., et al.Progrès de la recherche sur les matériaux biomédicaux modifiés par la polydopamine [J]. Modern Stomatology, En 2017,31(2): 113-116.
[30]Jiang S, Le Zhu R, Il a X, et Al., et al. amélioré photocytotoxicité De curcumine livré by solide lipid Les nanoparticules [J]. International Revue de presse De la Nanomédecine, En 2017, 12 ans: P. 167-178.
[31]Purpura M, Lowery RP, M. Wilson J., et Al., et al. Analyse des données De la Différents innovants formulations De la curcumin pour amélioré relative Biodisponibilité orale in human Sujets [J]. La communauté européenne Revue de presse De la Nutrition, À partir de 2018 57(3): 929-938.
[32] fr Y, Lu Lu Y, Lee RJ, et Al., et al. Nano encapsulé Curcumine: et its potentiel fOu bien biomédical Applications [J]. Revue internationale De la Nanomédecine, À partir de 2020, 15 ans: 3099-3120.
[33]Lewandowska U, U, Szewczyk K, Hrabec E, E,E, et Al., et al. Aperçu général Du métabolisme and bioavailability amélioration De la polyphénols [J]. J J J Agriculture et pêche La nourriture Chem, Chem, En 2013, 61(50): 12183-12199.
[34]Guimaraes-Stabili Monsieur, De M. Aquino Le SG, De Almeida Curylofo F, et al. systémique administration De la curcumin or Pipérine améliore the parodontale Réparation: a préliminaire étude in Rats [J]. Le Clin Par voie orale Investig, En 2019, 23(8): 3297-3306.
[35]Martin CA, CA, Paris, France G, Volk (en anglais) J, et al. Curcumin En combinaison with La pipérine supprime ostéoclastogenèse in Vitro [J]. Revue de presse De la L’endodontie, En 2015, 41(10): De 1638 à 1645.
[36]Barros CHN, CHN Accueil» Hiebner DW, Fulaz S, et al. synthèse and auto-assemblage De la curcumin-modifié amphiphile polymère Micelles avec antibacterial activity [J]. Revue de presse De la Nanobiotechnologie, 2021, Article 19(1): 104.
[37]Kang C, La vie de Jung E, Hyeon H, et al. Activable à l’acide Curcumine polymérique Les nanoparticules as thérapeutique agents pour Arthrose [J]. Nanomédecine: La nanotechnologie, Biologie, and Médecine, 2020, 23: les droits de l’homme 102104.
[38]Gupta A, Keddie DJ, DJ, Kannappan V, et al. La Production Et caractérisation De la bacterial cellulose hydrogels chargé Avec curcumine encapsulé in cyclodextrine as blessure Pansements [J]. La communauté européenne polymère Journal, 2019, 118: formation professionnelle 437 — 450.
[39]Nasra MM, Khiri (Khiri) Mon ami, Hazzah Eh bien, et al. Formulation, Caractérisation in vitro and clinique Évaluation des projets De la curcumin Gel in situ pour Le traitement De la Parodontite [J]. La drogue Livraison, En 2017, 24
(1): 133-142.
[40] Zhang ZhangXinjian, Zhang Bin. Progrès de recherche dans l’application de systèmes d’administration de médicaments à base de nanoparticules dans le traitement médicamenteux local de la parodontite [J]. Par voie oraleDisease Prevention and Control, En 2022,30(1): 73-76.
[41] il est C, Zhang X, Yan Yan R, et al. amélioration De la Efficacité du cisplatine by Lipid-CaO (2) Médié par nanoporteur Modulation complète De la the tumeur Microenvironnement [J]. Le Biomater Mon, 2019, 7(10): 4260-4272.
[42]Srivastava S, Mahomet. S, pantalon AB, AB,AB, et al. co-livraison De la 5- fluorouracile and curcumin nanohybride formulations Pour améliorer chimiothérapie contre oral squamous cellule Carcinome [J]. Revue de presse De la maxillo-faciale and Oral Chirurgie, À partir de 2018 17(4):597-610.
[43]Trigo-Gutierrez Je, Vega-chacemon emon Y, Soares AB, et Al. Antimicrobien activity De la curcumin in Nanoformulations: Un programme complet Revue [J]. International Revue de presse of Sciences moléculaires, 2021, 22(13): 7130.
[44] des S, Parandhaman T, À propos de Dey M.d. biomolécule Synthèse assistée of biomimétique nanocomposite hydrogel pour Hémostatique et blessure healing Application [J]. vert La chimie, 2021, 23
(7): 629-669.
[45]Ravishankar PL, PL, Kumar: Eh oui, Anila: Fr, EN, fr, it, nl, pt et al. effet of Application locale of curcumin and ornidazole gel in Parodontite chronique Patients [J]. International Revue de presse De produits pharmaceutiques Enquête, 2017, 7(4): 188-192.
[46]Pulikkotil S N.-é. Les effets of curcumin on créviculaire niveaux of IL ‐ 1β and CCL28 in expérimental Gingivite [J]. Dentaire australien Journal, 2015, 60(3): 317-327.
[47]Zhang Y, Huang Huang L, Mazurel D, et al. clinique efficacy De curcumine contre chlorhexidine as an adjuvant to Mise à l’échelle Et racine rabotage pour the Le traitement of Parodontite: A Revue systématique and Méta-analyse [J]. phytothérapie Recherche: PTR, 2021, 35(11): 5980-5991.
[48]Al-Maweri SA, Alhajj MN, Deshisha EA, EA, et al. Curcumine bains de bouche contre chlorhexidine in Le contrôle plaque Et gingivite: A systématique Revue de presse and Méta-analyse [J]. Int Int J Dent Hyg, 2022, 20(1): 53-61.
-
Précédent précédent
Etude sur l’utilisation de la poudre de curcuma dans les additifs alimentaires
-
Suivant:
Quelles sont les utilisations de l’extrait de curcuma en poudre de curcuma dans l’industrie alimentaire?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




