Natural Glutathione Ingredient for Next-Generation Dietary Supplement Upgrades
Against the backdrop of rapid growth in the Complément alimentaire market, consumers are demanding higher standards regarding product ingredient sourcing, scientific substantiation, and actual efficacy. The new generation of supplements must not only be safe and effective but also emphasize natural attributes and clear scientific mechanisms.
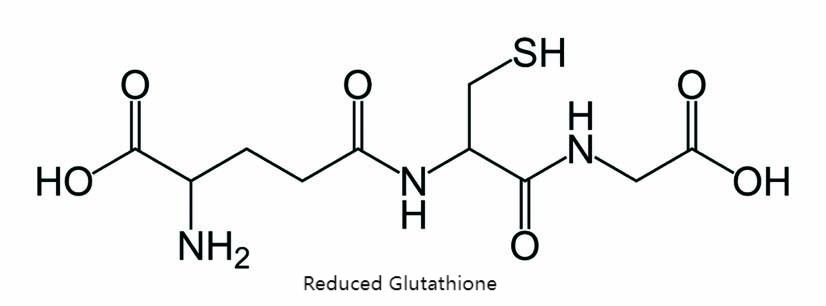
Within this trend, natural glutathione—an endogenous tripeptide in the human body—is gaining increasing attention for its unique physiological functions. Composed of glutamic acid, glycine, and cysteine linked by γ-amide bonds, it is widely present in animals, plants, and microorganisms, serving as a key component for maintaining cellular health and physiological balance.
Green Spring Technology specializes in supplying high-quality natural glutathione raw materials, dedicated to providing core support for dietary supplement upgrades. We rigorously control raw material sourcing and production processes to ensure products possess high purity, stable activity, and excellent biocompatibility, helping brands create more competitive functional products.
What Does Green Spring Technology's Natural Glutathione Raw Materials Offer You?
● Strengthen scientific backing for your products, enhancing formula professionalism
● Meet consumer demand for “clean label” and natural ingredients
● Provide more reliable raw material assurance for product development
● Establish a differentiated advantage in an increasingly homogenized market
We believe science-based raw material innovation will become a key force driving the advancement of the dietary supplement industry. Green Spring Technology is committed to collaborating with industry partners to pioneer a new chapter in dietary supplement development.
1 Green Spring Technology Natural Glutathione: Empowering Next-Generation Dietary Supplement Advancement with Scientific Core
Glutathione is a vital small-molecule peptide within living organisms, playing multiple core roles in cells through its unique structure. Green Spring Technology is dedicated to providing high-quality natural glutathione raw materials, transforming this natural wisdom of life into a reliable foundation for your product innovation.
1.1 Support Factor for the Intrinsic Defense System
Research indicates that glutathione is closely linked to maintaining the normal functioning of the body's defense system. It helps support the natural activity of multiple defense enzymes within the body, providing foundational support for the body's intrinsic protective mechanisms.
Green Spring Technology's Value Proposition: Our natural glutathione raw materials serve as the ideal functional ingredient for developing dietary supplements focused on “daily health maintenance” and “internal vitality support,” helping consumers build proactive, healthy lifestyles.
1.2 Guardian of Cellular Health
As a vital intracellular antioxidant molecule, glutathione directly participates in maintaining a healthy, reduced cellular environment. It helps counteract oxidative stress generated by daily metabolism and protects the integrity of cellular structures.
Green Spring Technology's Value Proposition: Through rigorous end-to-end quality control, we ensure high activity and stability of our glutathione, positioning it as the core ingredient for your “cellular nutrition” and “energy revitalization” concept products. This meets consumer demand for “inner-to-outer” health support.
1.3 Synergistic Enhancer for Nutritional Metabolism
Glutathione participates in multiple nutrient metabolic processes within the body. It has been shown to optimize the bioavailability of certain minerals (such as iron and selenium) and plays a role in amino acid transport and utilization, demonstrating exceptional synergistic potential.
Green Spring Technology's Value Proposition: Incorporating Green Spring Technology's glutathione into your multi-nutrient supplements, sports nutrition products, or foundational health formulas effectively enhances the scientific rigor and overall nutritional value of your formulations. It achieves synergistic benefits among ingredients, creating unique selling points for your products.
1.4 Active Regulator of Vitality and Performance
Glutathione is extensively involved in the body's energy metabolism cycle, serving as an indispensable component for maintaining metabolic vitality. It also shows promising research potential in supporting bodily function under specific conditions.
Green Spring Technology's Value Proposition: From “Metabolic Support” to “Condition Revitalization,” our natural glutathione raw materials open vast product innovation possibilities. We invite you to explore with us, transforming foundational research into next-generation health products that meet market demands.
Choosing Green Spring Technology means selecting a partner grounded in science and dedicated to product application innovation. Let us collaborate to advance the health evolution of dietary supplements.
2 Green Spring Technology Defines Excellence Through Precision Analysis
In the field of glutathione raw materials, precise testing and analysis are not merely quality control measures—they are fundamental guarantees of product efficacy and safety. Green Spring Technology understands that only ingredients validated by rigorous data can serve as reliable foundations for your product upgrades. Therefore, we have established a multidimensional testing system centered on high-performance liquid chromatography (HPLC), ensuring consistent excellence in every batch of raw materials we ship.
2.1 Why We Choose High-Performance Liquid Chromatography (HPLC) as Our Quality Control Cornerstone
Among various detection methods, electrochemical approaches are susceptible to interference, iodometric methods lack specificity, and fluorescence techniques rely on derivatization. Green Spring Technology steadfastly adopts the industry-recognized HPLC method because it delivers irreplaceable benefits for both us and you:
★ Precise Qualitative and Quantitative Analysis:
HPLC effectively separates glutathione from impurities like “molecular fingerprinting,” accurately determining its true content. This eliminates misidentification, ensuring precise formulation ingredients and authentic dosages.
★ Exceptional Stability and Reproducibility:
This method offers rapid analysis, high selectivity, and stable, reliable results—providing the technical foundation for our outstanding batch consistency. Choosing us means your products will enjoy long-term, stable market performance.
2.2 Green Spring Technology's Commitment: Transforming Testing Data into Your Core Competitive Advantage
We deeply understand the characteristics of various analytical methods, enabling us to build a quality control system that surpasses conventional standards:
2.2.1 Purity Assurance
Through our optimized HPLC analysis, we ensure effective separation of glutathione from impurities, delivering high-purity, premium raw materials that provide a pure foundation for your product efficacy.
2.2.2 Activity Preservation
We focus on the stability of the core functional group—the active sulfhydryl group. Through rigorous process control and testing, we maximize the retention of its biological activity, ensuring the raw material truly delivers results in your products.
2.2.3 Stable Supply
We have abandoned detection methods (such as high-performance capillary electrophoresis) that are only suitable for small samples and have low sensitivity. Instead, we have established stable and efficient quality control processes suitable for large-scale production, eliminating your concerns about stable production and supply.
At Green Spring Technology, rigorous testing is not the end point, but the starting point of trust. We are committed to transforming complex laboratory data into a simple and firm quality commitment in your hands. Choose us, and you gain a trusted raw material partner, jointly advancing dietary supplement quality and innovation to new heights.
3 Partner with Green Spring Technology to Innovate Dietary Supplements Together
As research into glutathione's physiological functions deepens, its core value in health maintenance becomes increasingly evident. Today, this key ingredient is transitioning from traditional applications toward a new generation of science- and innovation-driven health products.
Green Spring Technology precisely aligns with this trend through our high-quality natural glutathione raw materials. We are committed to being your reliable strategic partner, providing pure, potent, and stable core ingredients to upgrade your dietary supplements. Together, we meet market expectations for premium, science-based health solutions.
Let Green Spring Technology be your most dependable raw material partner as we jointly pioneer a new era in dietary supplements! Discover Green Spring Technology's full range of traceable glutathione solutions to infuse your products with stable competitiveness. Contact us today at helen@greenspringbio.com or WhatsApp: +86 13649243917 to embark on your product upgrade journey!
Références:
[1] Yang Changyan, Ba Qingyun, Zhang Zhixin, et al. Étude clinique sur le traitement de l’hépatite médicinale anti-tuberculose avec de l’alcool bicyclique combiné avec du glutathion réduit [J]. Médicaments modernes et cliniques,2017,32(04):653-656.
[2] SONG Zengting, JIANG Ning, ZHANG Aizhong, et al. Progrès des recherches sur les fonctions biologiques du glutathion [J]. Feed Research,2008(09):25-27.
[3] ZHOU Tingting, CAO Junming, HUANG Yanhua et al. Effets du glutathion alimentaire sur la croissance, les indices biochimiques tissulaires et les enzymes immunitaires non spécifiques chez le tilapia Jifu [J]. Journal of Aquatic Sciences,2013,37(05):742-750.
[4] Chang JG. Effets de la réduction du glutathion sur la fibrose du foie et la fonction immunitaire chez les patients atteints d’hépatite B [J]. China Practical Medicine,2019,14(35):124-126.
[5] Kritzinger E C. pratiques de vinification affectant les concentrations de glutathion dans le vin blanc [D]. Stellenbosch: université de Stellenbosch,2012.
[6] Cheng, YK. Détoxification du glutathion et de ses métabolites toxiques [J]. Avances in Biochemistry and Biophysics,1994(05):395-399+472.
-
Précédent précédent
Stable & Bioavailable: Liposomal Glutathione for Advanced Skin Brightening
-
Suivant:
Liposomal CoQ10 Powder: Maximizing Potency Retention and Shelf-Life Stability


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




