Quels sont les avantages pour la santé de Ginseng extrait Ginsenoside?
Le Ginseng is a traditional precious Chinese medicinal herb with a complex chemical composition and a wide range De labiological activities. With the advancement of modern separation and analysis techniques, the chemical composition of ginseng has been further elucidated. Ginsenosides are considered to be the madansactive substances in ginseng, accounting for about 4%. According to the different saponins, ginsenosides are divided into protopanaxadiol saponins, protopanaxatriol saponins and oleanolic acid saponins. So far, more than 40 ginsenoside monomers have been isolated and identified. In recent years, the pharmacological effects and mechanisms of ginsenosides have been widely studied. This article reviews the progress of pharmacological research on ginsenosides at home and abroad.

1 effets antitumoraux des ginsénosides
Au cours des 30 dernières années, la recherche sur l’activité antitumorale du ginseng et de ses proches a continué à s’approfondir, et divers ingrédients actifs antitumoraux tels que les ginsénosides Rg3, Rg1, Rh1, Rh2, et Rb1 ont été découvrés. Ces ingrédients ont montré un certain potentiel d’application clinique en favorisant l’apoptose des cellules tumorales, en inhibant la prolifération des cellules tumorales, en inhibant l’invasion et les métastases des cellules tumorales, en inhibant l’angiogenèse tumorale, en renversant la multirésistance des tumeurs, en affectant l’expression des gènes liés à la transduction du signal tumoral, et en améliorant l’immunité des patients avec la radiothérapie tumorale. En particulier, ils sont particulièrement importants dans la réduction des effets secondaires de la radiothérapie et de la chimiothérapie chez les patients tumeurs et l’amélioration de la sensibilité des cellules tumorales aux médicaments thérapeutiques.
Jin Yan et al. [1,2[traduction]ont constaté que le ginsénoside Rb1 peut améliorer significativement la fonction des cellules tueuses naturelles (NK) et la teneur en facteur de nécrose tumorale (TNF)-α en étudiant l’effet du ginsénoside Rb1 et Rg1 en association avec le 5-fluorouracile sur l’apoptose des lymphocytes spléniques chez les souris tumorales S180 induites par la dexaméthasone. Et antagonisé l’effet inhibiteur du 5-fluorouracile (P< 0,05). Jie Jian et al. [3] ont étudié l’effet du ginsénoside Rg3 sur l’expression du proto-oncogène Pim-3 et l’expression de la mauvaise protéine phosphorylée pBad (Ser112) et (Ser136). Il a été constaté que le ginsénoside Rg3 peut déréguler l’expression du Pim-3 et de la mauvaise protéine phosphorylée dans les cellules cancéreuses PANC-1 du pancréas, inhibant ainsi la prolifération des cellules PANC-1 et induisant l’apoptose.
Yoo JH et al. [4] studied the inhibitory effect of ginsenoside KG-135 On the proliferation of human prostate cancer cell lignées DU145 et PC-3 and tumor-bearing souris. Ils ont découvert que KG-135 peut inhiber de manière significative la prolifération des cellules DU145 et PC-3 en provoquant l’arrêt du cycle cellulaire à la phase G1. L’analyse immunohistochimique a montré que KG-135 pouvait réduire l’expression de l’antigène nucléaire cellulaire en prolifération (PCNA). Son mécanisme d’action peut impliquer l’inhibition du cycle cellulaire et la régulation de l’expression des gènes TNFRSF25 et ADRA2A. Liu TG et al. [5] ont étudié l’inhibition de l’angiogenèse et du cancer du poumon de souris par l’application combinée de ginsénoside Rg3 et de gemcitabine. Les résultats ont montré que la combinaison des deux a non seulement inhibé la croissance tumorale et amélioré le taux de survie et la qualité de vie des souris atteintes de cancer du poumon, mais a également médié de manière significative la nécrose tumorale, tout en inhibant l’expression du facteur de croissance endothélial vasculaire (VEGF) dans le sang et le tissu tumoral. Lee SY et al. [6] ont étudié l’effet du ginsénoside Rd sur l’inhibition des cellules cancéreuses du côlon HT29, ont constaté que le ginsénoside Rd a medié la régulation de 14 protéines mitotiques (stathmine 1, famille de protéines RP/EB associées aux microtubules et Stratifin) et était étroitement lié à des protéines liées à l’apoptose (inhibiteur de dissociation Rho GDP, tropomyosine 1 et annexine 5). On suppose que l’inhibition de la prolifération de la cellule cancéreuse du côlon HT29 par le ginsénoside Rd est liée aux protéines ci-dessus.
2 l’anti-alzheimer&#Effet des ginsénosides sur la maladie S (ma)
AD is a neurodegenerative disease that mainly occurs in early old age and old age. The main clinical manifestations of AD patients are memory loss and cognitifimpairment. Ginsenosides, the main active ingredient in ginseng, have anti-aging, memory-enhancing and geriatric disease-treating properties. They can increase the amount of acetylcholine (Ach) in the brain, increase the number of cholinergic nerve M receptors, and have a bidirectional regulatory effect on the central nervous system. They also have anti-inflammatory and antioxidant properties, protect nerve cells, reduce their apoptosis, and promote the synthesis of nucleic acids and proteins. In recent years, ginsenoside treatment of AD has been receiving increasing attention. Its mechanism is mainly related to promoting the activity of β-secretase and γ-secretase, which promote the formation of β-amyloid (Aβ), as well as protein phosphatase 2A, anti-oxidation and elimination of free radicals.
Wang YH et al. [7] studied the inhibitory effect of ginsenoside Rg1 on β-secretase activity and its protective effect on Aβ-induced cytotoxicity in PC12 cells in vitro. The results showed that ginsenoside Rg1 can inhibit β-secretase activity and protect PC12 cells from the damage caused by Aβ, such as lactate dehydrogenase (LDH) release, nitric oxide (NO) release, reactive oxygen species (ROS) production, lipid peroxidation, intracellular calcium elevation, and apoptosis. Li Yongkun et al. [8] [traduction] established an animal model of Tau protein hyperphosphorylation by injecting Okadaic acid into the dorsal hippocampus, and investigated whether Ginsénoside Rb1 has a relieving effect on Tau protein hyperphosphorylation.
Les résultats ont montré que le ginsénoside Rb1 peut réduire la surphosphorylation de la protéine Tau induite par l’acide okadaïque dans les neurones hippocampiens du rat, et le mécanisme pourrait être lié à l’augmentation de l’activité de la protéine phosphatase 2A. Shi YQ et al. [9] ont étudié l’effet du ginsénoside Rg1 sur le dépôt d’aβ et la capacité cognitive chez les souris vieillissant rapidement (SAMP8), ont constaté qu’après une administration à long terme de ginsénoside Rg1, les souris SAMP8 avaient significativement moins de dépôt d’aβ dans l’hippocampe, et des niveaux significativement plus faibles de PKARIIα dans l’hippocampe, tandis que les niveaux de la protéine cycliques phosphorylée de réponse monophosphate à l’adénosine (CREB) et du facteur neurotrophique dérivant du cerveau (BDNF) étaient significativement plus élevés. En outre, les capacités d’apprentissage et de mémoire des souris SAMP8 ont également été améliorées. Zhuang Ying et al. [10] ont étudié les effets du ginsénoside Rg2 sur les capacités d’apprentissage et de mémoire et la formation de la plaque sénienne (SP) dans un modèle de rat AD induit par Aβ25-35. Les résultats ont montré que les capacités d’apprentissage et de mémoire des rats du groupe d’administration préventive étaient augmentées par rapport au groupe modèle à chaque dose de ginsénoside Rg2, indiquant que le ginsénoside Rg2 a un certain effet protecteur sur les capacités d’apprentissage et de mémoire des rats AD et peut empêcher la formation de SP.

3. L’effet protecteur des ginsénosides sur l’ischémie cérébrale
L’avc ischémique est une maladie courante qui menace la santé humaine, avec les caractéristiques d’une incidence élevée, un taux d’invalidité élevé et un taux de mortalité élevé. Les saponines totales de Ginseng, le diol de ginsenoside ou les monomères de ginsenoside ont des degrés divers de dommages cérébraux anti-ischémiques. Les mécanismes actuellement acceptés comprennent la peroxydation des lipides anti-radicaux libres, la régulation de l’absence d’activité, l’augmentation du flux sanguin cérébral, la réduction de la neurotoxicité excitatoire des acides aminés, et l’inhibition de l’apoptose neuronale.
Chen LM et al. [11] ont étudié l’effet neuroprotecteur du ginsénoside Re sur les lésions d’ischémie-reperfusion cérébrale chez les rats. Les résultats ont montré que par rapport au groupe opératoire simulé, les symptômes neurologiques dans le groupe modèle étaient significativement augmentés, mais après l’administration de différentes doses de ginsénoside Re, les symptômes étaient atténués à des degrés divers. Il a également été détecté que le Re pouvait réduire significativement le gonflement mitochondrial et augmenter l’activité de l’adénosine-triphosphatéase. Des études ont montré que le ginsénoside Re a un bon potentiel neuroprotecteur contre les lésions d’ischémie-reperfusion cérébrale. Bao Cuifen et al. [12] ont étudié les effets et l’importance du ginsénoside Rg1 sur l’expression des protéines membranaires (saf) et des cystéines protéases (Caspase-3) dans le tissu cérébral de rats atteints d’avc ischémique. Les résultats ont montré que le nombre de cellules positives d’expression du saf et de la Caspase-3 dans le tissu cérébral des rats dans chaque groupe de doses de ginsénoside Rg1 et dans le groupe de médicaments positifs était significativement inférieur à celui du groupe modèle, ce qui indique que le mécanisme du ginsénoside Rg1 dans la prévention et le traitement des lésions ischémiques d’avc chez le rat pourrait être lié à l’inhibition de l’expression du saf et de la Caspase-3 dans le tissu cérébral. Hu Yu et al. [13] ont étudié l’effet protecteur de trois doses de ginsénoside Rb3 sur l’ischémie cérébrale focale chez les rats. Les résultats ont montré que le ginsénoside Rb3 avait un effet protecteur significatif sur l’ischémie cérébrale focale chez le rat. Les groupes à dose élevée, moyenne et faible ont tous considérablement atténué les symptômes comportementaux des rats atteints d’ischémie cérébrale, réduit le degré d’œdème cérébral, réduit la teneur en malondialdéhyde (MDA) dans le sérum, augmenté la teneur en superoxyde dismutase (SOD), réduit la zone d’infarctus cérébral et a atténué les dommages histopathologiques.
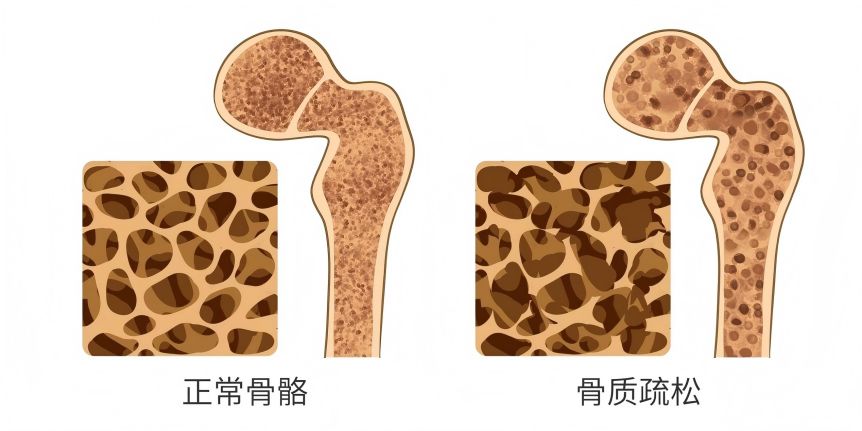
4 l’effet protecteur des ginsénosides sur les os
Avec le vieillissement de la société et de la population, l’incidence de l’arthrose et de l’ostéoporose augmente de jour en jour. De nombreuses études ont confirmé que les ginsénosides ont des effets semblables à ceux des œstrogènes et sont classés comme des phytoestrogènes [14]. Ils peuvent provoquer l’activation de la protéine kinase activée par mitogène cellulaire (MAPK) par des effets non génomiques de l’activation des récepteurs d’oestrogène, résultant en un effet ostéogénique. Lv Zhenchao et al. [15] [traduction] ont observé les effets des ginsénosides Rg1 et Rb1 sur l’apoptose induite par l’il-1 des chondrocytes in vitro et ont comparé les différences de leurs effets sur les cellules. Les résultats ont montré que les ginsénosides Rg1 et Rb1 avaient un effet inhibiteur significatif sur l’apoptose des chondrocytes et pouvaient inhiber l’apparition et le développement de l’arthrose du genou. Liu J et al. [16] [traduction]ont étudié l’effet du ginsénoside Rh2 sur la résorption osseuse induite par l’ostéoclaste. Les résultats ont montré que le ginsénoside 20(R)-Rh2 avait un effet inhibiteur sélectif sur la résorption osseuse sans cytotoxicité. Yang Renxuan et al. [17] ont étudié les effets du ginsénoside Rg1 sur la prolifération et l’expression des chondrocytes in vitro. Les résultats ont montré que le ginsénoside Rg1 pourrait augmenter la prolifération cellulaire, antagoniser l’interleukine (IL)-1α, réduire la SOD et dégrader le collagène de type II, indiquant que le ginsénoside Rg1 pourrait favoriser la prolifération des chondrocytes in vitro et l’expression de leur phénotype.
5. L’effet immunomodulateur des ginsénosides
Des études pharmacologiques modernes ont montré que les ginsénosides ont pour effet de réguler la fonction immunitaire du corps, et peuvent améliorer les fonctions immunitaires non spécifiques et spécifiques (y compris l’immunité cellulaire et l’immunité humorale) des animaux de laboratoire. Les observations cliniques ont montré que les ginsénosides peuvent améliorer ou réguler la fonction immunitaire du corps, et peuvent être utilisés ou utilisés en conjontion avec des troubles immunitaires. Zhang Shanyu et al. [18] ont étudié l’effet du polysaccharide d’astragale (APS) et du ginsénoside (TG) sur la prolifération des lymphocytes T du sang périphérique chez les personnes normales et sur la fonction immunitaire des souris traitées par cyclophosphamide (CY). Ils ont découvert que la combinaison du APS et du TG peut favoriser la prolifération des lymphocytes T du sang périphérique chez les personnes normales et améliorer la fonction immunitaire des souris, et a un certain effet synergique. Song X et coll. [19] [traduction]ont étudié l’effet adjuvant du ginsénoside Re sur la réponse immunitaire de souris induite par le sous-type inactivé du virus de la grippe H3N3. Les résultats ont montré que l’administration de ginsénoside Re augmentait significativement la réponse immunitaire des anticorps spécifiques du sérum IgG, IgG1, IgG2a et IgG2b. En même temps, l’indice immunitaire humoral (ih) et la prolifération des lymphocytes ont également augmenté de manière significative, indiquant que les cellules Th1 et Th2 étaient activées.
6 autres
En tant que l’un des principaux ingrédients actifs du ginseng, les ginsénosides ont divers effets pharmacologiques. En plus des effets pharmacologiques mentionnés ci-dessus, les ginsénosides ont également d’autres effets, tels que la baisse de la glycémie. Lai DM et al. [20] [en]ont utilisé un modèle de rat diabétique induit par la streptozotocine pour observer l’effet du ginsénoside Rh2 sur la glycémie. L’expérience a montré qu’après l’injection intraveineuse de Rh2 à des rats modèles à jeun pendant plus de 120 minutes, la glycémie a diminué, et cet effet hypoglycémique était dépendante de la dose. La recherche sur le mécanisme de l’effet hypoglycémique suggère que le ginsénoside Rh2 pourrait fonctionner en augmentant la sécrétion de β-endorphine. La β-endorphine active le récepteur μ-opioïde, ce qui peut conduire à une expression accrue du transporteur de glucose de type 4 (GLUT4). Les ginsénosides favorisent également la guérison des brûlures. Kimura Y et al. [21] [en]ont montré que le ginsénoside Rb1 isolé à partir de ginseng rouge favorise fortement la cicatrisation des brûlures chez les souris à de faibles concentrations. Cet effet de promotion peut être lié à l’expression accrue du facteur inductible de l’hypoxie (HIF) dans les kératinocytes et à l’augmentation de la teneur en IL-β causée par l’accumulation de macrophages au niveau des brûlures.
7 résumé
Ginsenosides, the main active substance in ginseng, ont un large éventail d’effets pharmacologiques, y compris l’activité anti-tumorale, l’activité du système nerveux, et l’activité du système cardiovasculaire. À l’heure actuelle, la plupart des recherches sur les ginsénosides sont précliniques, et des recherches plus approfondies sont nécessaires sur leurs effets cliniques.
Références:
[1] [traduction] Jin Yan, Qu Tingting, Liu Yuedong et al. Étude expérimentale sur les effets des ginsénosides Rb1 et Rg1 et du 5-fluorouracile sur l’apoptose des lymphocytes spléniques chez des souris porteurs de tumeurs S180 induites par la dexaméthasone [J]. Journal of Traditional Chinese Medicine, 2006, 24 (7): 1 272.
[2] [traduction] Qu Tingting, Jin Yan, Liu Yuedong, et al. Effets des ginsénosides Rb1 et Rg1 et du 5-fluorouracile sur la fonction immunitaire des souris porteurs de tumeurs [J]. Research in Chinese Medicine, 2006, 19(5): 16.
[3] [traduction] Jian Jie,Hu Zhi-Fang,Huang Yuan. Effet du ginsénoside Rg3 sur le Pim-3 et les mauvaises protéines dans le pancréas humain Lignée cellulaire cancéreuse PANC-1[J]. Chin J Cancer,2009,28(5): 461.
[4] [traduction] Yoo JH,Kwon HC,Kim YJ,et al. KG-135, enrichie en ginsénosides sélectionnés, inhibe la prolifération de cellules de cancer de la prostate hu- man en culture et inhibe la croissance de xénogreffes chez les souris athymiques [J]. Cancer Lett,2010,289(1):99.
[5] [traduction] Liu TG,Huang Y,Cui DD,et al. Effet inhibiteur du ginsénoside Rg3 combiné avec la gemcitabine sur l’angiogenèse Et la croissance du cancer du poumon chez la souris [J]. BMC Cancer,2009, 23(9):250.
[6] [traduction] Lee SY,Kim GT,Roh SH,et al. Changements protéomiques liés à l’activité anticancéreuse des cellules HT29 par le traitement du ginsénoside Rd[J]. Pharmazie,2009,64(4):242.
[7] [traduction] Wang YH,Du Gh. Le ginsénoside Rg1 inhibe l’ activité de la bêta-sécrétase in vitro et protège contre la cytose induite par l’ abeta. Totoxicité dans les cellules PC12 [J]. J Asian Nat Prod Res,2009,11 (7):604.
[8] Li Yongkun, Chen Xiaochun, Zhu Yuanyi et al. La saponine de Ginseng Rb1 réduit la surphosphorylation de la protéine Tau induite par l’acide okadaic dans les neurones hippocampiens du rat [J]. Acta Physiologica Sinica, 2005, 57 (2): 154.
[9] [traduction] Shi YQ,Huang TW,Chen LM et al. améliore cognitive La performance in Souris SAMP8 [J]. J AlzheimersDis,2010,19(3):977.
[10] ] Zhuang Ying, Shi Bo, Tian Xin et al. Effets du ginsénoside Rg2 sur l’apprentissage et la capacité de mémoire et la formation de plaque sénile chez les rats atteints d’alzheimer' modèle de maladie S [J]. Chinese Journal of Gerontology, 2010, 30(2): 202.
[11] [traduction] Chen LM,Zhou XM,Cao YL,et al. Neuroprotection du ginsénoside Re dans les lésions d’ischémie-reperfusion cérébrale chez le rat [J]. J Asian Nat Prod Res,2008,10(5~6):439.
[12] Bao Cuifen, Liu Xia, Liang Jia, et al. Effets du ginsénoside Rg1 sur l’expression des protéines du saf et de la Caspase-3 dans le tissu cérébral de rats atteints d’avc ischémique [J]. Journal of Liaoning University of Traditional Chinese Medicine, 2009, 11(5): 211.
[13] Hu Yu, Chen Haofan, Zang Linquan, et al. Effet protecteur du ginsénoside Rb3 sur l’ischémie cérébrale focale chez le rat [J]. Journal de l’université pharmaceutique de Guangdong, 2008, 24(5): 590.
[14] [traduction] Chan RY,Chen WF,Dong A,et al.effets semblables à l’oestrogène du ginsénoside Rg1 dérivé de Panax notoginseng[J]. J ClinEndocrinol Metab,2002,87(8):3 691.
[15] Lv Zhenchao, Guo Yanxing, Cao Xiangyang, et al. Effets des ginsénosides Rg1 et Rb1 sur l’apoptose des cellules du cartilage du genou cultivées in vitro [J]. World Journal of Integrative Medicine, 2010, 5(1): 32.
[16] Liu J,Shiono J,Yu H,et al. 20(R)-ginsenoside Rh2, pas 20(S), est un inhibiteur sélectif de l’ostéoclastgenèse sans Toute cytotoxicité [J]. Bioorg Med Chem Lett,2009,19(12): 3 320.
[17] Yang Renxuan, Wang Zhaopei, Xu Shucai, et al. Effets du ginsénoside Rg1 sur la prolifération et le phénotype des chondrocytes [J]. New Chinese Medicine and Clinical Pharmacology, 2004, 15 (1): 4. [18] Zhang Shanyu, Pu Huisun, Shen Yingai. Une étude préliminaire sur l’effet immunomodulateur du polysaccharide d’astragale en association avec des saponines de ginseng [J]. Chinese Pharmacy, 2005, 16 (21): 1 620.
[19] Song X,Chen J,Sakwiwatkul K,et al. Amélioration des réponses immunitaires au vaccin antigrippal (H3N2) par ginsen- oside Re[J]. Int Immunopharmacol,2010,10(3):351.
[20] Lai DM,Tu YK,Liu M,et al. Médiation de la β-endorphine par le ginsénoside Rh2 pour abaisser le glucose plasmatique chez les rats diabétiques induits par le streptozotociné.plantamed,2006,72(1):9.
[21] Kimura Y,Sumiyoshi M,Kawahira K,et al. Les effets of Saponines de ginseng isolées de racines de ginseng rouge sur brûlure Cicatrisation des plaies chez la souris [J]. Br JPharmacol,2006,148(6): 860.
-
Précédent précédent
Ginseng extrait Ginsenoside et régulation immunitaire
-
Suivant:
Quelle est la méthode d’extraction du ginsénoside?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




