Quelle est la méthode d’extraction du ginsénoside?
Le Ginseng («Panax»Le ginsengC. Le temps de travailA. Meyer) is a perennial herb in Le conseil des ministresfamily Araliaceae. It is a traditional precious Chinese medicine avecthe effects De latonifying qi Et en plusproducing blood, strengthening the positive Et en plusdispelling the negative. Ginsenosides are one De lathe main active ingredients in ginseng, accounting pourabout 4% De lathe total mass De laginseng. They have the effects De laenhancing the human immune system, anti-aging, anti-fatigue, Et en plustreating cardiovascular diseases, and have now become the main ingredient in some special effect medicines. ExtractiSur leand séparationtechnology is crucial to the efficient extractionand La concentrationDe laGinsénosides deginseng and the purification of preparations Par:removing as many impurities as possible. This paper reviews the reported extractionand separation methods of ginsenosides, avecthe aim of providing a reference for the extraction and separation of ginsenosides.

1 méthodes d’extraction des ginsénosides
1.1 méthodes traditionnelles d’extraction
1.1.1 méthode d’ébullition
The decoction La méthodemainly uses water as the extraction solvent. The medicinal material is heated and boiled for a certain period of time to obtain a decoction. This needs to be repeated many times and is mainly used to extract the better water-soluble components of Chinese herbal medicines. It is suitable for medicinal materials whose active ingredients are soluble in water and not sensitive to heating. It is one of the earliest and most commonly used extraction methods for extracting Chinese herbal medicine components. Chen Ali et al. used the extraction rates of ginsenosides Rb1, Re, and Rg1 as the evaluation indicators, and used an orthogonal test method to optimize the boiling extraction conditions of ginseng. The results showed that the highest extraction rate of ginsenosides was obtained by boiling 8 times the mass of ginseng in water for 2 times, each time for 1 hour [1].

1.1.2 méthode de macération
La méthode de macération consiste à extraire les principes actifs des matériaux médicinaux par immersion dans un solvant à température ambiante ou dans des conditions chauffées selon le principe de dissout like. Zhang Chunhong et al. ont utilisé une méthode de macération avec une température d’extraction de 60 °C, un temps de macération de 2 h et un volume de solvant 10 fois plus élevé que le macérat pour extraire les ginsénosides, avec un rendement maximal total de saponine de 8,33 % [2]. Sun Guangzhi et al. ont déterminé le processus d’extraction optimal en étudiant les effets du solvant multiple, du temps d’extraction, du nombre d’extractions et de la fraction volumique du solvant sur le taux d’extraction du propanoyl ginsénosides [3].
1.1.3 méthode de Reflux
Dans la méthode de reflux, un solvant organique est utilisé comme solvant d’extraction. Le solvant volatil est distillé en chauffant la matière médicinale, puis condensé et retourné à l’extracteur pour poursuivre le cycle d’extraction jusqu’à ce que les principes actifs soient complètement extraits. Actuellement, l’opération traditionnelle au reflux pour l’extraction des ginsénosides en laboratoire consiste à reflux avec 80% de méthanol à (75 ± 1) °C pendant 3 h et à répéter 4 fois. Yan Guangjun et al. ont utilisé la teneur totale en ginsénosideRg1 et ginsenoside Re ReRecomme indice, et par la comparaison et l’analyse complète de plusieurs processus, il a été démontré que le processus d’extraction par reflux était le plus efficace [4]. Zhang Ling et al. ont étudié l’effet de différents procédés d’extraction sur la teneur en composants efficaces dans le ginseng et ont déterminé les conditions optimales du processus d’extraction pour l’extraction par reflux [5]. Hao Shaojun et al. ont utilisé la teneur en ginsénosides comme indice d’évaluation et ont utilisé la méthode d’essai orthogonale pour optimiser le processus d’extraction optimal [6]. Kim et al. ont utilisé l’extraction de saponines de type diol et triol comme indice pour optimiser le processus optimal pour la méthode de reflux d’éthanol [7].
1.1.4 méthode d’extraction Soxhlet
The medicinal material is packed in gauze or filter paper and placed in the Soxhlet extraction extraction vessel. A certain amount of extraction solvent is added to the flask, heated and kept boiling. The solvent vapor condenses and refluxes into the extraction vessel to come into contact with the medicine. After that, the active ingredients dissolve in the solvent. After the solvent reaches a certain volume, the solvent that has dissolved the active ingredients is refluxed into the flask. the solvent is reheated and evaporated, and after cooling, it is re-exposed to the medicine to extract it in a cycle. Zhang Jing et al. took 2 g of ginseng powderEt 60 mL Lde méthanol ont été ajoutés. Après extraction dans un extracteur Soxhlet pendant 8 h, la teneur totale en saponine de ginseng a été mesurée par spectrophotométrie et a été de 3,27 % [8] [traduction]. Wood et al. ont utilisé la méthode d’extraction Soxhlet à une température de 80 à 90 °C pour extraire efficacement les ginsénosides [9]. Qu et al. ont placé 500 mg d’échantillon de ginseng américain dans un extracteur de Soxhlet et ont extrait des ginsénosides avec 70% d’éthanol [10].
1.2 méthodes modernes d’extraction
1.2.1 extraction par fluide supercritique
Un état monophasé formé lorsque la température et la pression dépassent le point critique d’une substance est appelé un fluide supercritique. Les fluides supercritiques ont une densité similaire à celle des liquides, une faible viscosité et une forte diffusivité, ce qui leur donne une solubilité relativement forte et permet une extraction efficace avec un transfert de masse rapide. Zhang Le et al. ont utilisé l’extraction par fluide supercritique pour extraire les ginsénosides Rh1 et Rh2 [11] [traduction]. Luo et al. ont utilisé l’extraction de fluide supercritique assistée par ultrasons pour obtenir des ginsénosides avec un rendement élevé [12]. Wood et al. ont utilisé le méthanol et le DMSO comme modificateurs pour l’extraction par fluide supercritique des ginsénosides du ginseng américain, extrait 90% des saponines totales [9]. Wang et al. ont constaté que le rendement de ginsénosides extraits par fluide supercritique augmentait avec l’augmentation de la température [13].

1.2.2 méthode de séparation de la mousse
La méthode de séparation par mousse est une technique qui utilise les différences dans les propriétés d’adsorption des substances à la surface des bulles pour les séparer. Comme les saponines à ginseng ont les propriétés d’un tensioactif, elles peuvent produire une mousse stable lorsqu’elles sont agitées ou que du gaz est passé, de sorte qu’elles peuvent être séparées et enrichies à l’aide de la technologie de séparation par flottation. Xiu et al. ont utilisé la méthode de séparation par mousse pour séparer et concentrer cinq types de saponines, y compris Rb1et Rb2 [14]. Zhang Dajia et al. ont utilisé la séparation par mousse pour isoler les ginsénosides Rb1, Rb2, Rd, Rc et Rf [15]. Wang Yutang et al. ont utilisé la flottation en mousse dynamique pour isoler et enrichir les ginsénosides de type diol dans l’extrait de ginseng [16]. Zhang et al. ont utilisé une extraction en flottaison de mousse en phase solide pour isoler les saponines traces de la racine de ginseng américain [17].
1.2.3 extraction assistée par ultrasons
Ultrasonic-assisted extraction is a process that applies the combined effects of cavitation, vibration, crushing, and agitation generated by ultrasound to traditional Chinese medicine extraction to achieve efficient and rapid extraction. Zhang Chongxi et al. compared the traditional methods of water decoction, warm soaking, ethanol reflux, microwave-assisted extraction, and ultrasonic-assisted extraction, and the results showed that the ultrasonic method was the best [18]. Zhang Xianchen et al. used orthogonal design to determine the content of ginsenosides under different ultrasonic treatment conditions by colorimetry, and optimized the ultrasonic extraction process of ginsenosides [19]. Wu et al. found that ultrasonic-assisted extraction with water, methanol, and n-butanol as solvents at 38.5 kHz is three times faster than traditional extraction [20].
1.2.4 technologie d’extraction assistée par micro-ondes
L’extraction assistée par micro-ondes utilise des micro-ondes pour chauffer le solvant dans le système d’extraction, de sorte que les principes actifs de l’échantillon de plante extrait soient séparés et pénètrent dans le solvant en contact avec celui-ci. Cette technologie utilise principalement l’effet de chauffage par micro-ondes pour compléter le processus d’extraction et de séparation. L’énergie micro-ondes absorbée par la substance extraite provoque une élévation rapide de la température interne de la cellule, ce qui entraîne la rupture de la cellule et la dissolution des principes actifs dans le solvant.
Kwon et al. ont optimisé les conditions pour l’extraction assistée par micro-ondes des saponines de ginseng à l’aide de la méthode de la surface de réponse [21]. Shu et al. ont étudié les effets de l’intensité des micro-ondes, du temps d’extraction et d’autres facteurs sur l’extraction assistée par micro-ondes [22]. Shi et al. ont utilisé l’extraction assistée par micro-ondes pour isoler sept types de ginsénosides, y compris Rg1, Re et Rb1 et sept autres ginsénosides des racines de ginseng à l’aide de l’extraction assistée par micro-ondes [23]. Wang et al. ont utilisé une extraction assistée par micro-ondes sous pression pour extraire des racines de ginseng et des échantillons de ginseng d’amérique, et ont étudié les effets du temps d’extraction, de la pression et du solvant sur le rendement d’extraction [24]. Shi Wei et al. ont utilisé la technologie d’extraction assistée par micro-ondes pour extraire et séparer rapidement et efficacement six ginsénosides, Rg1, Re, Rb1, Rc, Rb2, et Rd, de la racine de ginseng [25].
1.2.5 extraction à haute et à ultra-haute pression
L’extraction haute pression et ultra-haute pression (au-dessus de 100 MPa) applique une pression hydrostatique à un mélange de solvant d’extraction et de médecine traditionnelle chinoise. Une fois que la pression à l’intérieur et à l’extérieur des cellules végétales atteint l’équilibre, la pression est rapidement libérée, ce qui entraîne la perméabilisation des cellules. Les principes actifs dans les cellules passent à travers les différentes membranes des cellules et sont transférés à la solution d’extraction extracellulaire, atteignant ainsi l’objectif d’extraction des principes actifs. L’extraction supercritique permet d’obtenir la plus grande efficacité d’extraction dans les plus brefs délais. Si l’opération est effectuée correctement, un extrait pur peut être obtenu et l’extraction peut être effectuée à température ambiante, ce qui favorise la séparation des substances thermiquement instables.
L’extraction à haute pression et supercritique a été appliquée dans l’extraction des ginsénosides. Chen Ruizhan et al. ont utilisé l’extraction supercritique pour extraire les ginsénosides dans les conditions d’un solvant à 50% d’éthanol, une pression de 500 MPa, un temps d’extraction de 2 min en utilisant la méthode d’ultra-haute pression [26]. Chen et al. ont utilisé une pression ultra-élevée pour extraire les ginsénosides à température ambiante et ont optimisé les conditions du procédé d’extraction en utilisant la méthode de conception uniforme [27]. Lee et al. ont comparé les rendements des ginsénosides totaux et des métabolites du ginsénoside dans des conditions d’extraction à haute pression et d’extraction thermique, et ont montré que le rendement de l’extraction à haute pression était plus élevé [28].
1.3 nouvelles méthodes
1.3.1 méthode d’extraction biomimétique
La méthode d’extraction biomimétique est basée sur les principes de base du métabolisme des médicaments et utilise une simulation in vitro du système gastro-intestinal pour extraire les ginsénosides. Chen Xin et al. ont utilisé de la poudre ultrafine de ginseng comme matière première et ont extrait des ginsénosides avec des solvants biomimétiques et de l’eau comme solvant d’extraction [29] [en]. Les résultats ont montré que l’efficacité d’extraction des ginsénosides totaux, du ginsénoside Rg1 et du ginsénoside Re par la méthode d’extraction biomimétique était plus élevée que celle par la méthode d’extraction à l’eau, et le chromatogramme de l’extrait biomimétique a montré la production de nouveaux composants.
1.3.2 méthode d’extraction par champ électrique pulsé
The pulsed electric field extraction method is a new extraction method that has been applied in food engineering to extract active ingredients À partir debiological materials. Hou et al. used pulsed electric field extraction to extract ginsenosides Rg1, Re, Rb1, Rc, Rb2, and Rd À partir deginseng, and compared the method with hot reflux extraction and microwave-assisted extraction. The results showed that pulsed electric field extraction had the highest yield and the shortest time [30].
1.3.3 extraction par dispersion en phase solide dans la matrice
Le procédé d’extraction par dispersion en phase solide consiste d’abord à mélanger l’échantillon avec un dispersant abrasif, puis à charger le mélange dans une colonne de verre, et enfin à éluer et à extraire avec un solvant approprié. Shi et al. ont utilisé l’extraction par dispersion en phase solide pour l’extraction des feuilles de ginseng, en extrayant 8 ginsénosides tels que Rb2, Rc et Rd, et en les comparant à la méthode du reflux à chaud. Les résultats ont montré que la méthode d’extraction par dispersion en phase solide avait un rendement plus élevé, prenait moins de temps et consommait moins de solvant [31].
2 méthodes de séparation
2.1 séparation solide-liquide
Les ginsénosides sont généralement séparés par chromatographie solide-liquide. L’échantillon est extrait une ou plusieurs fois avec du méthanol ou de l’éthanol, puis l’extrait est recueilli, combiné et extrait par séchage sous vide. Les résidus en suspension dans l’eau sont séparés en fractions par différents solvants organiques, tels que la couche de n-hexane, d’acétate d’éthyle, de n-butanol et d’eau. La couche de n-hexane contient des impuretés de poids moléculaire élevé et solubles dans l’huile, tandis que les autres fractions sont ensuite séparées en parties plus petites par chromatographie sur une colonne de résine macroporeuse et une colonne de gel de silice à l’aide d’un système de solvant à gradient. Les fractions sont ensuite soumises à une séparation ultérieure par chromatographie sur colonne de gel de silice en phase normale, chromatographie sur colonne de gel de silice en phase inverse, chromatographie sur colonne de gel et élution par gradient avec différents systèmes de solvant. Les substances séparées peuvent être purifiées par chromatographie liquide préparatoire et leurs structures peuvent être déterminées par des méthodes chimiques et spectroscopiques.
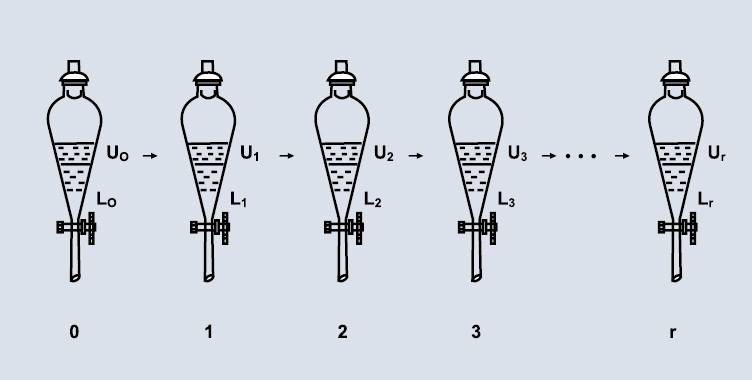
2.2 séparation liquide-liquide
La technologie de séparation liquide-liquide repose sur les différents rapports de séparation des échantillons dans des solvants non miscibles pour les séparer. Comme il n’y a pas de support solide, le problème de l’adsorption irréversible de la phase stationnaire sur l’échantillon de la chromatographie classique sur colonne est évité. Le cloisonnement liquide-liquide comprend principalement la chromatographie à contre-courant à grande vitesse et la chromatographie à partitioncentrifuge.
2.2.1 chromatographie à contre-courant rapide (HSCCC)
La chromatographie à contre-courant à grande vitesse (HSCCC) est largement utilisée dans la préparation et la séparation des ginsénosides. Avant la séparation HSCCC, l’échantillon de ginseng est extrait avec des réactifs organiques, et la fraction de saponine est concentrée et enrichie en passant à travers une colonne de résine macroporeuse, une colonne C-18 en phase inverse et une colonne liquide à moyenne pression chromatographie. La sélection efficace des conditions HSCCCcomprend le choix d’un système de solvant à deux phases et la méthode d’élution de l’échantillon. Le choix de la phase mobile est particulièrement important. Les applications récentes de HSCCC à la séparation des ginsénosides dans les produits à base de ginseng ont abouti à l’isolement des ginsénosides Rb1 [32-34], Rg1 [32,34,37], Re [32,34,37], Rf [33], Rd [33-34], Rg3 [35], Rg5 [35], Rk1 [35], F4 [35] et Ro [36].
2.2.2 chromatographie à partition centrifuge (CPC)
La chromatographie par séparation centrifuge (CPC) est une chromatographie de séparation liquido-liquide sans adsorption qui fonctionne dans un champ gravitationnel continu. Actuellement, le système de solvant chloroforme-méthanol-eau a été utilisé avec succès dans le CPC pour séparer les saponines. Wang et al. ont utilisé le CPC pour séparer les ginsénosides Rc, Rb1 et Re du ginseng américain à l’aide d’un système de solvant acétate d’éthyle n-butanol eau (1:1:2) [38].
2.3 nouvelles méthodes
2.3.1 adsorption sélective au charbon actif
Kuang et al. ont utilisé l’adsorption sélective au charbon actif pour séparer et purifier le ginsenoside Re des boutons de fleurs de ginseng [39].
2.3.2 technologie de démodulation
The composition and function of ginseng Sont habituellement étudiées en utilisant l’une des deux méthodes suivantes: «essai biologique de séparation» ou «essai biologique de séparation guidée». Afin de prouver que le composant extrait est biologiquement actif, un extrait sans le composant doit être préparé en tant qu’extrait dénaturé. Dans le processus de comparaison des activités biologiques, si l’activité biologique de l’extrait dénaturé est inférieure à celle de l’extrait original, cela signifie que le composant est une substance biologiquement active. Par conséquent, la méthode d’obtention de l’extrait démodifié est l’un des centres de recherche, y compris la chromatographie chimique et la chromatographie d’immunoaffinité.
2.3.2.1 chromatographie chimique
Some demulcent extracts can be prepared by column chromatography. For example, in order to prepare the Rb1 demulcent extract, the ginseng flower bourgeonextract is first separated through a macroporous resin column En utilisantwater and aqueous ethanol as the eluent. The aqueous ethanol stream is then separated by reverse-phase high-La performanceliquidechromatography. The separation can be divided into three parts: the water part, the Rb1 part, and the other saponin part. The Rb1 part is removed, and the remaining water part and other saponin parts are combined to form the Rb1 demoulding extract. In order to improve efficiency, Liu et al. invented an online control chromatographietechnique to prepare the demoulding extract [40].
2.3.2.2 chromatographie immunoadsorbante
La chromatographie immunoadsorbante est une méthode chromatographique dans laquelle la phase stationnaire est un anticorps monoclonauxdirigé contre le composé cible. C’est une méthode efficace pour séparer et enrichir les composants traces de mélanges complexes. La sélectivité élevée de la chromatographie d’immunoaffinité pour les composés cibles provient des protéines réticulées à la phase stationnaire. Tanaka et al. ont préparé des anticorps monoclonaux contre les ginsénosides Rb1 [41-43], Rg1 [44], Rd [45] et Re [46].
Par rapport à la méthode chromatographique chimique de préparation de l’extrait, la méthode chromatographique d’immunoaffinité augmente la sélectivité de l’analyse, réduit les étapes de préparation de l’échantillon et augmente le volume du support d’échantillon. Par contre, il réduit considérablement le temps nécessaire à la séparation chromatographique et le temps nécessaire pour choisir les conditions expérimentales optimales. Cependant, la méthode chromatographique d’immunoaffinité présente également quelques inconvénients, à savoir la complexité du procédé de préparation des anticorps monoclonaux et l’instabilité de la colonne d’immunoaffinité.
3 perspectives
Bien que les méthodes traditionnelles d’extraction et de séparation (décoction, reflux, etc.) aient chacune leurs propres avantages, elles présentent des limites telles que de longues durées d’extraction, une faible efficacité, une forte consommation de solvants et ne favorisent pas l’extraction de composants thermiquement stables ou volatils. Par conséquent, les gens ont cherché des méthodes plus efficaces et plus pratiques. Avec le développement continu de la technologie d’extraction de la médecine traditionnelle chinoise, de nouvelles méthodes appropriées pour l’extraction et la séparation des ginsénosides sont constamment émergent. Ils ont les avantâgesde temps d’extraction court, faible utilisation de solvant organique, sélectivité plus forte de l’extrait, et moins de pollution environnementale. Cela fournit une base pour le développement ultérieur et l’utilisation efficace des ginsénosides, et on pense que l’extraction, la séparation, et le développement ultérieur et l’utilisation des ginsénosides auront un avenir plus large.
Références:
[1] Chen A-li, Cui Y-xia, Zhou L-yan, et al. Optimisation du procédé d’extraction de l’eau de ginseng par méthode d’essai orthogonale [J]. China Modern Drug Application, 2009, 3 (9): 21-22.
[2] Zhang C-hong, Zhang C-xi, Zheng Y-lan, et al. Etude du procédé optimal d’extraction des ginsénosides par macération [J]. Journal of Jilin Agricultural University, 2003, 25 (1): 73-74, 78.
[3] Sun Guangzhi, Wang Jiyan, Liu Zhi, et al. Recherche sur le procédé optimal d’extraction des ginsénosides propanoyl du ginseng à l’aide d’expériences orthogonales [J]. Chinese Herbal Medicine, 2006, 37 (8): 1194-1195.
[4] Yan Guangjun, Zhang Baojiang, Xu Daojuan. Étude Comparative de plusieurs procédés d’extraction du ginseng couramment utilisés [J]. Shandong Pharmaceutical Industry, 2002, 21 (4): 8-8.
[5] Zhang Ling, Shan Weihua, Liang Ruixue et al. Recherche sur le processus d’extraction du ginseng [J]. Shizhen Traditional Chinese Medicine, 2000, 11 (9): 777-778.
[6] Hao Shaojun, Zhang Zhengchen. Méthode de conception orthogonale pour l’étude du procédé optimal d’extraction des ginsénosides [J]. Chinese Journal of Practical Medicine, 2007, 6(1): 48-50.
[7]Kim S J,Murthy H HN,Hahn E J,et al. Ginseng C.A.Meyer) [J]. Separation and Purification Technology, 2007,56(3) :401-406.
[8] Zhang Jing, Chen Quancheng, Gong Xiaojie et al. Effet des différentes méthodes d’extraction sur le taux d’extraction des ginsénosides [J]. Journal of Jilin Agricultural University, 2003, 25 (1): 71-72.
[9]Wood J A,Bernards N ° de catalogueA,Wan W K,et al.Extraction de ginsénosides De ginseng nord-américain utilisant du carbone supercritique diox- ide modifié [J]. The Journal of Supercritical Fluids,2006,39(1) :40-47.
[10]Qu C L,Bai Y P,Jin X Q,et al.étude sur les ginsénosides dans différents Parties et pièces détachées ages of «Panax»quinquefolius L.[J]. La nourriture Chemistry, 2009,115 (1) : 340-346.
[11] Zhang Le, Song Fengrui, Wang Qi, et al. Extraction supercritique de dioxyde de carbone des ginsénosides rares du ginseng [J]. Applied Chemistry, 2010, 27 (12): 1483-1485.
[12]Luo D L,Qiu T Q,Lu Q. Extraction assistée par ultrasons de ginsen- osides en supercritique Émissions de CO2 inverser Microémulsions [J]. Revue de presse De the Science of Food and Agriculture,2007,87 (3) :431-436.
[13]Wang H C,Chen C R, Chang C J. Extraction de dioxyde de carbone de gin- seng root cheveux huile and Ginsenosides [J]. La nourriture Chimie,2001,72 (4) : 505-509.
[14]Xiu Z L,Zhang D J,Jia L Y,et al.Foam séparation des ginsénosides De Panax ginseng[J]. The Chinese Journal of Process Engineering, 2001,1 (3) : 289-293.
[15] Zhang Daijia, Xiu Zhilong, Lin Xinhua, et al. L’effet des méthodes de séchage sur l’extraction et la séparation des ginsénosides du ginseng frais [J]. Journal of Integrated Traditional Chinese and Western Medicine, 2004, 2 (4): 292-294.
[16] Wang Yutang, Liu Xuebo, Yue Tianli, et al. Séparation et enrichissement des ginsénosides de type diol dans l’extrait de ginseng par flottation dynamique en mousse [J]. Journal of Chemical Sciences in Colleges and Universities, 2009, 30 (9): 1713-1716.
[17]Zhang D, Zhang H Q,Wu L W,et Al. Mousse flottaison -SPE for separation and concentration of tracer Ginsenosides [J]. Chroma- tographia,2010,72(1 /2) : 39-46.
[18] Zhang Chongxi, Zheng Youlan, Zhang Chunhong et al. Optimisation du procédé d’extraction des saponines totales de ginseng par différentes méthodes [J]. Ginseng Research, 2003, 15 (4): 5-8.
[19] Zhang Xianchen, Wang Shumin, Chen Guang et al. Etude du procédé d’extraction par ultrasons des saponines totales de ginseng [J]. Research and Practice of Modern Traditional Chinese Medicine, 2005, 19(6): 55-57.
[20]Wu J,Lin L,Chau F T. Extraction assistée par ultrasons du ginseng Saponines provenant de racines de ginseng et de cellules de ginseng cultivées [J]. Ultrason- ics Sonochemistry,2001,8 (4) : 347-352.
[21]Kwon j. H., [unused_word0006] langer j. M., paremon. Optimisation de l’extraction assistée par micro-ondes (MAP) pour les composants de ginseng par surface de réponse Méthodologie [J]. Journal of Agricultural and Food Chemistry,2003, 51 (7) : 1807 -1810.
[22]Shu Y Y,Ko M Y,Chang Y S., S., S. Micro-onde assisté extraction Des ginsénosides de la racine de ginseng [J]. Microchemical Journal,2003,74 (2) : 131 -139.
[23]Shi W,Wang Y T,Li J,et al.Investigation des ginsénosides dans différentes parties et âges de Panax ginseng[J]. Chimie alimentaire,2007,102 (3) : 664-668.
[24]Wang Y T,You J Y,Yu Y,et al.analyse des ginsénosides dans le ginseng Panax dans l’extraction assistée par micro-ondes à haute pression [J]. Food Chemistry,2008,110(1) : 161 -167.
[25] Shi Wei, Wang Yutang, Quan Xinjun et al. Détermination des ginsénosides dans la racine de ginseng par chromatographie liquide haute performance - détection par dispersion de la lumière par évaporation [J]. Analytical Chemistry, 2006, 34 (2): 243-246.
[26] Chen Ruizhan, Zhang Shouqin, Wang Changzheng. Recherche sur l’optimisation du procédé d’extraction des ginsénosides du ginseng par ultra-haute pression au moyen d’expériences orthogonales [J]. Chinese Herbal Medicine, 2005, 36(3): 365-368.
[27]Chen R Z,Meng F L,Zhang S Q,et al.effets des conditions d’extraction à très haute pression sur les rendements et l’activité antioxydante du ginsénoside du ginseng[J]. Separation and Purification Technology,2009,66 (2) : 340-346.
[28]Lee H S,Lee H J,Yu H J,et al.une comparaison entre haute pression hydrostatique extraction Et extraction de chaleur de ginsenosides from Ginseng (Panax ginseng C.A.Meyer) [J]. Journal of the Science of Food and Agriculture,2011,91 (8) : 1466 -1473.
[29] Chen Xin, Hu Chaoqi, Zhang Hongchang, et autres Etude préliminaire sur l’extraction des ginsénosides par chimie biomimétique [J]. Chinese Pharmacy, 2012, 23 (19): 1752-1754.
[30]Hou J G,He S Y,Ling M S,et al. Une méthode d’extraction des ginsen- osides du ginseng Panax par champ électrique pulsé [J]. Journal of Separation Science,2010,33 (17 /18) : 2707-2713.
[31]Shi X L,Jin Y R, Liu J B,et al. Dispersion en phase solide matrice ex- traction des ginsénosides dans les feuilles de Panax ginseng C.M.Mey [J]. Food Chemistry,2011,129(3) : 1253 -1257.
[32]Du Q Z,Jerz G,Waibel R, et al.Isolation De dammarane Les saponines De Panax notoginsengpar chromatographie à compteur à haute vitesse [J]. Journal of Chromatography a,2003,1008 (2) : 173 - 180.
[33]Qi X C,Ignatova S,Luo G,et al.isolement préparatoire et purification des ginsénosides Rf,Re,Rd and Rb1 from the Les racines of Panax Ginseng avec un système de sel/contenant des solvants et une étape de flux de gradi- ent par haute performance Contre - courant chromatographie couplé Avec un détecteur de diffusion de la lumière par évaporation [J]. Journal of chroma-tography a,2010,1217 (13) : 1995-2001.
[34]Cao X L,Tian Y,Zhang T Y,et al. Notoginseng, racine of Panax notoginseng (Burk.) F. H. : Chen, par HSCCC couplé with évaporatif lumière dispersion Détecteur [J]. Revue de presse of liquide Chromatographie & Related Technologies, 2003,26(9 /10) : 1579 -1591.
[35]Ha Y W,Lim S S,Ha I J,et al.isolement préparatoire de quatre ginsen- osides de coréen rouge Ginseng (Panax ginseng traité à la vapeur) C. A.Meyer), par chromatographie à courant à compteur à grande vitesse, avec détection par dispersion de la lumière par évaporation [J]. Journal of Chro- matography a,2007,1151 (1 /2) : 37-44.
[36]Cheng Y J,Liang Q L,Hu P et al. Combinaison de phase normale Moyenne - pression liquid chromatographie Et haute performance Chromatographie à contre-courant pour la préparation du ginsenoside - Ro De Panax ginseng à haute récupération et efficacité [J]. Séparation et Purification Technology,2010,73 (3) : 397-402.
[37]Chen F Q,Luo J G,Kong L Y. Isolement rapide des ginsénosides Re et Rg1 des racines de Panax ginseng par HSCCC -ELSDcombiné Avec MCI gel CC guidé par HPLC -MS[J]. Journal of Liquid Chro-
Matographie &; Related Technologies,2012,35 (7) : 912-923.
[38]Wang J,Bai H L,Liu C M,et al.Isolation et purification de gin- sénosides à partir d’extrait de plante de panax quinquefolium L. Par haute performance centrifuge partition chromatography couplé with ELSD [J]. Chromatographia,2010,71 (3 /4) : 267-271.
[39]Kuang P Q,Wang G,Yuan Q P,et al.séparation et purification du ginsenoside Re from ginseng bud Par sélectif Adsorption de Charbon actif et préparation Haute performance Chromatographie liquide [J]. naturelProduct Research,2012,26(3) : 286-290.
[40]Liu Y,Zhou J L,Liu P,et al.Chemical markers' Pêche et knock- out pour une activité holistique et une évaluation de l’interaction des composantes Dans les plantes médicinales [J]. Journal de chromatographie A,2010,1217 (32) : 5239-5245.
[41]Tanaka H,Fukuda N,Yahara S,et al.isolement du ginsénoside Rb1 de Kalopanax À propos de pictus by l’est buvard En utilisant Anti - -ginsénoside Rb1 monoclonaux Anticorps [J]. phytothérapie Research,2005,19 (3) : 255-258.
[42]Fukuda N,Tanaka H,Shoyama Y. Isolement de la pharmacologiquement Saponine active ginsenoside Rb1 du ginseng par immunoaffinité col- umn Chromatographie [J]. Revue de presse of Natural Produits,2000,63 (2) : 283-285.
[43]Putalun W,Fukuda N,Tanaka H,et al colonne d’immunoaffinité pour i- solation de Bioactif bioactif composés En utilisant Anticorps monoclonaux [J]. Journal de chromatographie liquide & Technologies connexes,2002,25 (13 /15) : 2387-2398.
[44]Tanaka H,Fukuda N,Shoyama Y. Formation d’anticorps monoclonal Contre un composant majeur du ginseng, le ginsénoside Rb1 et sa caractérisation [J].Cytotechnology,1999,29(2) : 115 -120.
[45]Morinaga O,Fukuda N,Tanaka H,et al.résolution chromatographique De glucosidique Composés, ginsénosides on polyéthersulphone Mem - brane, et son application à l’immunodosage quantitatif du ginseng Saponines [J]. Glycobiology,2005,15 (10) : 1061 -1066.
[46]Morinaga O,Tanaka H,Shoyama Y. Détection et quantification du ginsénoside Re dans des échantillons de ginseng par un chromatographique Immuno - method using monoclonal anticorps contre ginsenoside Re [J]. Journal of Chromatography. B, Technologies analytiques dans la Biomedical and Life Sciences,2006,830(1) : 100 -104.
-
Précédent précédent
Ginseng extrait Ginsenoside et régulation immunitaire
-
Suivant:
Étude sur différents Types d’extrait de Ginseng Ginsenoside


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais




