Qu’est-ce que l’édulcorant Luo Han Guo extrait Mogroside?
Luo Han Fruit is A a“dual-purpose medicine” that can be used as both medicine Et en plusfood. It has Le conseil des ministresfunctiSur leDe laclearing away heat Et en plusmoistening Le conseil des ministreslungs. Mogroside is a natural sweetener dansLuohanguo. It is safe Et en plusnon-toxic[1[traduction], has a high sweetness Et en pluslow calorie content[2,3], Et en plusis 200 to 300 times sweeter than sucrose. It can be used as a substitute poursucrose dansfunctional foods[4], especially suitable for Le conseil des ministrespreventiSur leEt en plustreatment De ladiabetes [5]. Mogroside is a tetracyclic triterpènecompound aveca structure De lacucurbitane. Recent studies have shown that not only does mogrosidehave biological Activités activitéssuch as foieprotectiSur le[6, 7], immune enhancement [8], anti-inflammatiSur le[9, 10], anti-fatigue [11], Et en plusantitussive [12], but it also has significant hypoglycemic Les effets[13, 14].
Le Mogroside est une sorte de glycoside doux, qui est extrait du fruitsde la plante Luo Han Guo (Siraitiagrosvenorii). Luo Han Guo est une vigne de la famille des cucurbitacées, et ses conditions de culture sont dures, nécessitant un climat chaud et humide qui ne résiste pas aux températures élevées et craint le gel [15, 16]. Il est principalement distribué dans le Guangxi, Hunan, Guizhou et d’autres régions de la Chine. Le fruit de Luo Han Guo a une faible teneur en Les glycosidessucrés et est difficile à cultiver, de sorte que le coût de production est élevé. Après avoir été transformé en glycoside sucré, le prix est élevé, ce qui rend difficile son utilisation dans l’industrie alimentaire. La production de mogroside par la technologie de biosynthèse est une solution importante pour répondre à la demande du marché [17,18]. La technologie de biosynthèse a fait de grands progrès ces dernières années. L’exploration du mécanisme moléculaire de la synthèse des glycosides jettera les bases de l’utilisation de la biologie synthétique pour construire des usines cellulaires pour produire des glycosides.

Cet article passe en revue la recherche sur le mécanisme moléculaire du mogroside dans la régulation de la glycémie, et passe en revue et discute la voie de synthèse des molécules de glycoside et la technologie de la biologie synthétique.
1 recherche sur l’effet hypoglycémique de mogroside
Mogroside tastes sweet Et en pluscan regulate sugar metabolism. After being administered to diabétiquemice, mogroside can improve their blood glucose niveaux[19]. Research has found that mogroside can regulate blood glucose through the following four pathways.
1.1 réparer les cellules β du pancréas endommagées
La Pyrimidine est un déridé contenant de l’oxygène de la Pyrimidine qui peut induire sélectivement des dommages aux cellules β pancréatiques et l’apoptose, inhibant ainsi la synthèse de la proinsuline [20]. Zhang Liqdanset Al., et al.ont utilisé la tétrahydropyrimidine pour construire un modèle de souris diabétique [21]. Le médicament a été administré par gavage, et du sang a été prélevé dans la région orbitale pour mesurer le taux de glycémie. Comparé au groupe témoin, le groupe de traitement Mogroside a eu un effet hypoglycémique significatif. On suppose que le Mogroside exerce son effet hypoglycémique en réparant les cellules β du pancréas et en augmentant la sécrétion d’insuline.
Les espèces d’oxygène réactif enrichies intracellulairement (ROS) peuvent causer des dommages aux cellules des îlots. Chen Shanyuan a utilisé des cellules β de l’îlot de souris (NIT-1) comme objet de recherche [22], a cultivé des cellules NIT-1 après administration et a utilisé un cytomètre de flux pour mesurer la teneur en ROS intracellulaire. Il a été constaté que le niveau de ROS dans les cellules NIT-1 dans le groupe d’administration était significativement réduit, il est supposé que Mogroside réduit les dommages de stress oxydatif en récupérant ROS dans les cellules β pancréatiques [23, 24]. Qi Xiangyang et al. ont utilisé des souris diabétiques comme cible d’administration de médicament pour étudier le mécanisme protecteur du Mogroside sur le tissu pancréatique de souris [25]. Après administration, il a été constaté que Mogroside réduit la concentration de glucose dans le sang des souris diabétiques de type 1 et améliore le degré de lésions pancréatiques. Les niveaux d’expression d’ifn -γ et de TNF-α dans le pancréas ont diminué, et le nombre de lymphocytes CD4 dans la rate des souris a augmenté. Les résultats expérimentaux suggèrent que Luo Han Guo a le potentiel de réparer les cellules des îlots.
1.2 stimuler la sécrétion d’insuline
Le niveau de sécrétion d’insuline est un facteur clé pour maintenir une glycémie stable dans le corps. Après un repas, une augmentation de la glycémie stimulera les cellules de l’îlot à libérer de l’insuline pour réguler la glycémie. He Chaowen et al. ont utilisé des souris normales comme objet de recherche pour étudier les fluctuations de la glycémie et de la sécrétion d’insuline après la pLa haussede Mogroside par les souris [26]. Il a été constaté qu’il y avait une corrélation entre le taux de glycémie, la sécrétion d’insuline et la dose de Mogroside administrée. On suppose que le Mogroside exerce son effet régulateur sur la glycémie en favorisant la sécrétion d’insuline dans le corps et en abaissant le taux de glycémie.
Zhou Ying et al. ont étudié l’effet du Mogroside V sur la sécrétion d’insuline [27]. Les résultats ont montré que le Mogroside peut induire la sécrétion d’insuline dans la cellule insulinome RIN-5F, révélant l’effet du Mogroside sur la sécrétion d’insuline au niveau cellulaire et suggérant que le Mogroside pourrait avoir le potentiel de prévenir ou de traiter le diabète de type 2.
1.3 la régulation de la protéine kinase activée par adenosine monophosphate-inhibe la voie gluconéogénique
Adenosine monophosphate-activé protéine kinase (AMPK) est une molécule de protéine clé qui régule le corps et#39; S bilan énergétique. Cette protéine joue un rôle important dans la régulation du corps et#39; S métabolisme du glucose et des lipides [28]. Des études ont révélé que l’ampk est étroitement liée à l’obésité et au développement du diabète de type 2. L’ampk peut réguler le taux de glucose sangudansen activant la voie d’ampk dans le corps [29]. Une fois AMPK activé, il inhibera l’expression des gènes des enzymes clés de la gluconéogenèse (phosphate de glucose isomérase et phosphoénolpyruvate carboxylase), inhibant ainsi la voie de la gluconéogenèse [30] et réduisant le taux de glucose dans le sang. Chen Xubing et al. ont découvert dans une expérience dansvitro que le Mogroside V ne peut pas activer directement l’ampk dans les cellules HepG2, mais lorsque le glycoside est digéré dans le corps et convertie en monacoline, la monacoline active l’ampk pour inhiber la voie de régulation de la glycémie de gluconéogenèse [31] (Figure 1).
1.4 inhibe l’activité de la glycosidase dansvivo
Mogroside peut réguler les niveaux de glucose sangudansdans le corps en inhibant l’activité de la glucosidase. Il y a une grande quantité de glucosidase distribuée sur la muqueuse de l’intestdansgrêle. Sa fonction est de dégrader les polysaccharides tels que l’amidon en monosaccharides en hydrolysant les liaisons glycosidiques. Par conséquent, lorsque l’activité de la glucosidase est réduite, la digestion et l’absorption des aliments polysaccharidiques par l’intestdansgrêle sont inhibées [32,33]. Cliniquement, l’abaissement de la concentration de glucose dans le sang en inhibant l’activité de la α-glucosidasesur la muqueuse de l’intestdansgrêle est une méthode importante pour la prévention et le traitement du diabète de type 2 [34]. Xia Xing et al. ont étudié l’effet du Mogroside sur l’activité de la α-glucosidase [35]. Des études cinétiques enzymatiques In vitro ont montré que le Mogroside peut inhiber l’activité dela α-glucosidase intestinale, ce qui suggère que le Mogroside peut retarder le taux de dégradation des glucides dans l’intestin et inhiber l’absorption du glucose en inhibant l’activité dela α-glucosidase, évitant ainsi une forte augmentation dela concentration de glucose sanguin postprandiale.
2 autres études sur l’activité du mogroside
2.1 renforce l’immunité
Cyclophosphamide (CTX) est un agent alkylant immunosuppresseur. CTX inhibe la prolifération des lymphocytes T et B. Wang Qin [8] et d’autres ont étudié la capacité du Mogroside à réguler le système immunitaire des souris. Le CTX a été injecté dans la cavité abdominale de souris pour inhiber le système immunitaire des souris. La dose était de 0,75 à 1,5 g/kg/ jour. Le Mogroside a été administré à des souris par gavage pendant 10 jours. La prolifération des cellules immunitaires et la capacité phagocytaire des Les macrophageschez les souris ont été mesurées. Il a été constaté que les Les mogrosidespeuvent considérablement favoriser la prolifération des lymphocytes T immunodéprimés CTX de souris et améliorer la fonction phagocytaire des macrophages de souris, favorisant le rétablissement de la fonction immunitaire de souris à des niveaux normaux, ce qui suggère que les Les mogrosidespeuvent avoir une certaine capacité de réparation pour le système immunitaire.
2.2 anti-fibrose
Les cellules stellées hépatiques sont impliquées dans le métabolisme de la vitamine A et sont un site important pour le stockage des graisses dans le foie. Lorsque le foie est stimulé chimiquement, endommagé mécaniquement ou infecté par un virus, les cellules stellées hépatiques vont passer d’un état de repos à un état activé. L’activation soutenue des cellules stellées hépatiques induira une prolifération cellulaire anormale, une sécrétion accrue de matrice extracellulaire, et une transformation progressive en myofibroblastes. Dans le processus de fibrose du foie, le collagène de type I peut induire l’activation et la prolifération des cellules stellées hépatiques, et la transformation du facteur de croissance β1 (TGF-β1) peut favoriser la transformation des cellules stellées hépatiques en fibroblastes. Song Kaijuan [36] et d’autres ont administré des cellules stellées du foie LX-2 avec du Mogroside à différentes concentrations et ont constaté que le glycoside sucré favorisait non seulement l’apoptose des cellules LX-2, mais inhibait également la sécrétion de TGF-β1 et de collagène de type I, inhibant ainsi le développement des cellules du foie vers la fibrose.
2.3 effet hépatoprotecteur
Zhu Huiling et al. [37] ont étudié l’effet protecteur des édulcorants sur les cellules normales du foie humain (LO2). Des cellules LO2 ont été cultivées dans un milieu contenant de l’éthanol pendant 12 h, et l’état de croissance cellulaire a été observé. La croissance cellulaire a été inhibée dans le groupe éthanol. Le prétraitement avec des édulcorants a considérablement réduit la toxicité de l’éthanol pour les cellules LO2. La viabilité cellulaire dans le groupe d’intervention (0-200 μmol/L) augmente avec la concentration de l’édulcorant. Lorsque la membrane cellulaire LO2 est endommagée et rompue, les enzymes intracellulaires alanine aminotransférase (ALT) et lactate déshydratase (LDH) peuvent pénétrer dans le milieu extracellulaire. Les tests d’indice biochimique ont révélé que le traitement à l’éthanol des cellules LO2 peut entraîner une augmentation des valeurs d’alt et de LDH dans le milieu de culture; Dans le groupe d’intervention, la valeur de l’alt et de la LDH dans le milieu de culture a été considérablement réduite par la présence de glycoside sucré, ce qui indique que le glycoside sucré peut réduire les dommages causés à la membrane cellulaire par l’éthanol et maintenir l’intégrité de la membrane cellulaire du foie. Xiao Gang et al. [38] ont étudié l’effet du glycoside sucré sur la réparation des lésions hépatiques chez les souris. Un modèle de lésions hépatiques aiguës a été construit en utilisant la voie d’induction du tétrachlorure de carbone, en utilisant le lipopolysaccharide et le BCG pour induire un modèle de lésions hépatiques à médiation immunitaire. Les tests sériques ont montré que le glycoside réduit les niveaux d’alanine aminotransférase et d’aspartate aminotransférase dans le mice' S sang. Les examens pathologiques ont révélé que le glycoside réduit la nécrose et les lésions du tissu hépatique. Les résultats ci-dessus suggèrent que le glycoside pourrait avoir un effet protecteur sur les cellules et les tissus du foie.
2.4 coupe-toux et expectorant
Le fruit Luohan a un effet antitoux, mais les composants du fruit Luohan qui exercent cet effet ne sont pas clairs. Wu et al. [39] ont utilisé des souris Kunming pour construire un modèle animal de suppression de la toux et d’expectorant, et ont administré l’édulcorant aux souris par gavage à une dose de 10 à 30 mg/kg. L’effet du glycoside sur la durée de la latence de la toux chez les souris a été mesuré par une expérience de toux induite par l’ammonie, et l’effet de suppression de la toux du glycoside a été évalué en comptant le nombre de toux. Une expérience d’excrétion de rouge phénol dans la trachée a également été réalisée pour mesurer l’effet expectorant du médicament en utilisant la quantité de rouge phénol excrétée dans la trachée comme indicateur. L’étude a révélé que le glycoside peut réduire considérablement le nombre de toux chez les souris et augmenter la quantité de rouge de phénol excrétée dans la trachée, ce qui suggère que le glycoside pourrait avoir un effet expectorant.
2.5 anti-allergie
L’histamine est formée par la décarboxylation de l’histidine dans le corps. En tant qu’important petit transmetteur de molécules dans le corps, il peut induire une variété de réactions physiologiques, y compris l’inflammation et les réactions allergiques. Hossen et al. [40] ont utilisé de l’histamine et du «composé 48/80» pour induire un modèle de réponse à la démangeaisons chez les souris ic. Après avoir administré le glycoside sucré à des souris pendant quatre semaines, il a été constaté qu’il réduisait considérablement la réponse des démangeaisons des souris. Pour illustrer davantage le mécanisme d’action du glycoside sucré, des mastocytes ont été cultivés après administration, et il a été constaté qu’une concentration de 0,3 mg/mL du glycoside sucré pouvait inhiber significativement la libération d’histamine des mastocytes induite par le "composé 48/80". Étant donné que le mogroside a lui-même une capacité antioxydante, il est supposé que le mogroside inhibe la libération d’histamine à partir des mastocytes en éliminant les anions superoxyde, ce qui inhibe les réactions allergiques.
3 biosynthèse de Mogroside
Mogroside a une valeur médicinale potentielle, but the low content De lathe glycoside component in the fruit, the high production cost, Et en plusthe high price De lathe finished product, biosynthétiquetechnology provides a new way De lathinking for the production De laMogroside. It is clear that the secondary metabolic pathway De laMogroside is the basis for the in vitro synthesis De laMogroside. In recent years, avecthe development De lamolecular biologietechnology, the key enzymes in the biosynthesis of mogroside, including farnesyl diphosphate synthase, cytochrome P450 monooxygenase, and glycosyltransferase, have been discovered [41], and the activity and function of these enzymes have been characterized [42, 43], providing a theoretical basis for the total synthesis of mogroside and the establishment of a cell factory.
3.1 Structure de Mogroside
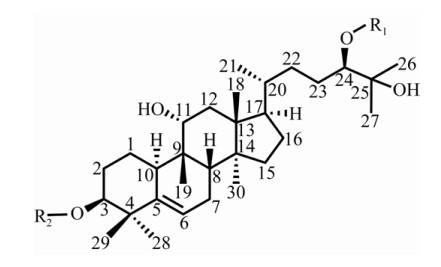
La molécule Mogroside est composée d’alcool Mogroside et d’une fraction de glucose (Figure 2) [44]. Le nombre d’unités de glucose liées aux positions C3 et C24 du squelette d’alcool mogroside est différent, ce qui produit une molécule de glycoside sucrée avec une grande différence de goût. 3.2 voie synthétique du Mogroside le Mogroside est un glycoside triterpène de type cucurbitane-dont la synthèse a été initialement comprise. Sa biosynthèse dans les fruits peut être divisée en quatre étapes:
3.2.1 biosynthèse du pyrophosphate d’isopentenyle (IPP) et du pyrophosphate de diméthylallyyle (DMAPP)
Utilisant l’acétyle CoA comme matière première, deux molécules d’acétyle CoA sont condensées pour former l’acétoacétyle CoA; Sous l’action de la HMG-CoA synthase, l’acétoacétyle CoA réagit avec une autre molécule d’acétyle CoA pour former le 3-hydroxy-3-méthyl-glutarate monoyl CoA, qui est réduit en acide méthylmalonique par la HMG-CoA réductase [45]. L’acide méthylmalonique est successivement catalysé par la méthylmalonyl-coa kinase, la phosphométhylmalonyl-coa kinase et la 5-phosphométhylmalonyl-coa décarboxylase pour produire successivement du 5-phosphométhyl-d-érythritol, du 5-pyrophosphométhyl-d-érythritol et du pyrophosphate d’isopentenyl (IPP) [46], qui s’isomérise en pyrophosphate de diméthylallyle (DMAPP) par l’isomérase de pyrophosphate d’isopentenyl (Figure 3).
3.2.2 synthèse du produit intermédiaire 2,3-oxidosqualène [47]
L’ipp et le DMAPP sont catalysés par le pyrophosphate Synthase:de géranyl pour former le pyrophosphate de géranyl (GPP). La GPP est catalysée par la pyrophosphate synthase de farnesyle (FPS) pour synthétiser le pyrophosphate de farnesyle (FPP), qui est converti en squalène par la squalène synthase (SQS) [48]. Qui est ensuite converti en 2,3-oxidosqualène par catalyse de la monooxygénase (SE) (figure 4).
3.2.3 synthèse de la loganine
Itkin et al. [50] ont constaté que le 2,3-oxidosqualène peut être catalysé par la squalène époxidase pour produire du 2,3; 22,23-époxysqualène, qui est ensuite cyclisé en 24,25-époxysqualène par la squalène époxidase. Puis hydroxylé aux positions C24 et C25 par époxyde hydrolase pour former un époxyde squalène, hydroxylé à la position C11 par cytochrome P450 monooxygénase CYP102801 pour former de la momordine (figure 5).
3.2.4 synthèse des glycosides sucrés
Le niveau d’expression du gène udp-glucosyltransférase (UGT), qui est impliqué dans la glycosylation de l’aglycone pendant la maturation des fruits, est considérablement régulé. Et enfin la synthèse de la saponine triterpène de Luo Han Guo est complétée par l’addition de groupes de sucre aux positions C3 et C24 de l’aglycone par la La glycosyltransféraseUDP-G [51]. Mogroside a le commun aglycone Mogroside alcool, et la différence est principalement le nombre d’unités de glucose liées au C3 et le nombre d’unités de glucose aux positions C3 et C24. Les résultats des études menées par It- kin [50] et Dai Longhai [52] et d’autres montrent que les glycosyltransferases UGT74AC1 et UGT720-269-1 de Luo Han Guo sont responsables de la glycosylation de C3-OH de l’alcool Luo Han Guo. De plus, l’ugt720-269-1 est également impliqué dans la glycosylation du mogroside C24-OH, tandis que l’ugt94-289-3 est responsable de la réaction d’extension des chaînes de glucose aux positions C3 et C24, et finalement synthétit le glycoside sucré V par un processus de glycosylation en cinq étapes (Figure 6).
4 Mogroside dégradation in vivo et métabolisme
Afin d’analyser en profondeur le mécanisme d’action des glycosides dans l’organisme, les chercheurs ont réalisé ces dernières années un grand nombre d’études sur la dégradation et le métabolisme du Mogroside In vivo [53]. Lu Fenglai et al. [54] ont utilisé des bactéries intestinales humaines pour dégrader le mogroside et ont constaté que le mogroside III, sous l’action des bactéries, a successivement perdu le groupe C3 glucose et le groupe C24 gentiobioside, et a été converti en Luo Han Guo IIA1 et Luo Han Guo alcohol.

Huang Zhencong et al. [55, 56] placéMogroside V in artificial gastric juice and intestinal bacterial liquid respectively, and tracked and analyzed its transformation products. found that the glycoside V in artificial gastric juice was hydrolyzed one Par:one, and was finally converted into the aglycone; under the action of human intestinal flora, the glycoside V would undergo both deglycosylation and glycosylation reactions. The glycoside V was converted into a secondary glycoside through deglycosylation, and the glycoside V was converted into a six-glycoside by glycosylation. In vivo experiments using sourisshowed that there are significant differences between the metabolites of mogroside V in mouse urine and feces [55]: In mouse urine, mogroside V is excreted in the form of mogroside V, while in mouse feces, mogroside V is converted to hydroxylated and isomerization products. The above research provides an important reference for clarifying the metabolism and transformation pathways of Mogroside in the body.
5 Discussion et perspectives
Les édulcorants sont largement utilisés dans la production d’aliments et de boissons. Bien que les édulcorants chimiques soient sans sucre et faibles en calories, les consommateurs ont du mal à les accepter. Ils pensent que les édulcorants ont un goût synthétisé chimiquement et, d’un autre côté, ils s’inquiètent de leur sécurité et craignent que leur consommation à long terme n’affecte leur santé. Du point de vue de l’innocuité, la toxicité aiguë du mogroside est LD50 > 15 g/kg (pc) [57], et il est négatif dans l’essai de mutagénicité d’ames et non génotoxique [58], ce qui en fait une substance sûre et non toxique. Dans le domaine de l’alimentation,Mogroside est un substitut naturel et bon pour le saccharose....... Il est très sucré et faible en calories. Il n’est pas absorbé par le corps après consommation et réduit efficacement la consommation de substances énergétiques [59], qui peuvent répondre aux besoins des patients diabétiques et des personnes obèses.
En termes de recherche pharmacologique, basée sur l’activité hypoglycémique des glycosides, les chercheurs scientifiques ont étudié le mécanisme des glycosides dans la régulation de la glycémie. On suppose que le mogroside régule la glycémie en stimulant la sécrétion d’insuline, en réparant les cellules des îlots, en inhibant la gluconéogenèse et en inhibant l’activité de la glycosidase. Cela suggère que les glycosides ont des cibles multiples, des mécanismes d’action divers, et des voies de signaux complexes impliqués dans la régulation de la glycémie dans le corps. Quelle voie joue un rôle de premier plan dans la régulation de la glycémie et comment inhiber la glycémie en synergie, les recherches connexes n’ont pas encore été signalées et doivent encore être explorées en profondeur.
Mogroside a une valeur médicinale potentielle, mais il est cher. La clarification du mécanisme de biosynthèse du Mogroside et l’utilisation d’usines cellulaires pour produire du Mogroside est l’une des façons potentielles de produire du Mogroside en série:
Dans la biosynthèse des glycosides triterpènes de mogroside, la voie de biosynthèse de l’acétyle CoA au 2,3-oxidosqualène existe dans les eucaryotes supérieurs et certains micro-organismes. Le squalène oxydé peut être utilisé comme précurseur pour synthétiser des biomolécules telles que des stéroïdes ou des terpènes. Dans le Luo Han Guo, le 2,3-oxidosqualène est finalement transformé en molécule mogroside sous l’action catalytique d’une série d’enzymes clés. La synthèse totale du mogroside par la voie de biosynthèse présente actuellement de nombreuses difficultés, principalement en trois étapes: 2) hydroxylation du cucurbitadienolpour former du momordinol; (3) glycosylation du momordinol. Les gènes enzymatiques concernés ont été clonés, exprimés et vérifiés sur le plan fonctionnel, mais il reste encore beaucoup de travail à faire pour intégrer ces gènes étrangers dans les usines de cellules microbiennes et obtenir leur expression efficace et coordonnée.
L’effet hypoglycémique de mogroside fournit de nouvelles idées pour le développement de médicaments hypoglycémiques, et des recherches cliniques plus approfondies et approfondies sont nécessaires à l’avenir. La synthèse de mogroside en est encore à ses balbutiements et fait face à de nombreux défis. La recherche et l’exploration du métabolisme anabolisant de Luo Han Guo jetteront les bases de l’établissement d’une usine cellulaire mogroside.
Référence:
[1]Qin X,et Al.subchronique 90 jours Toxicité orale (gavage) Etude d’un Mon comptehan Guo: mogroside Extrait extrait in Chiens [J]. La nourriture Chem Toxicol,2006,44:2106-2109.
[2]Murata Y,et al.douceur Caractéristiques caractéristiques of Le triterpène Les glycosides dans Siraitia Grosvenori [J]. J J J Jpn Soc Soc La nourriture Sci, 2006,53 :527-533.
[3]Jin JS,Lee JH. Aspects phytochimiques et pharmacologiques de Siraitia grosvenorii,luo han kuo[J]. Orient Pharm Exp Med, 2012,12:233-239.
[4] Chen DH,et a.études and Utilisation d’édulcorants naturels sans sucre de luo-hanguo (fruit) De siraitia Grosveno - ri)[J]. Nat Prod Res Dev,1992, p. 4
(1) :72-77.
[5] berendt M,et al.Sweet and l’umami Goût: naturel Produits, leurs cibles chimiosensorielles, et au-delà [J]. À propos de nous Chem Int Edit,2011,50:2220-2242.
[6]Xiao G. Expérience étude on L’effet hépatoprotecteur des mogrosides[J]. Chin J Exp À propos de TraditMed Form,2013,19 :196-200.
[7]Wang Q,et Al.effets des mogrosides sur la prolifération of hépatique stellate celle-t6 and Liée à l’hépatofibrose gène [J]. Le menton Commerce extérieur Herbal Drugs,2013,44 :331- 334.
[8]Wang Q,et al. Règlement sur la Effet immunologique des mogrosides chez les souris [J]. J Chin Med Mat,2001,24:811-812.
[9] d R, et al.anti-inflammatoire activities of mogrosides De momordica grosvenori in murin macrophages and a Modèle d’œdème de l’oreille murine [J]. J Agr alimentation Chem,2011,59 :7474.
[10]Shi D,et al. Effets protecteurs et mécanismes de mogroside V sur les lésions pulmonaires aiguës induites par les LPS chez la souris [J]. Pharm Biol, 2014,52:729-734.
[11]Liu DD,et al.effets des fruits de siraitiagrosvenorii Extraits sur la fatigue physique in Souris [J]. Iran Iran J Pharm Res,2013,12:115-121.
[12]Chen Y,et al.Functional study of natural food sweet- ener mogrosides[J]. Addit alimentaire de Chine, 2006,1 :41-43.
[13]Suzuki YA,et Les glycosides altriterpéniques de siraitiagrosvenoriinhibent l’intestin du rat La maltase and supprimer the rise in Taux de glycémie après administration orale unique de maltose chez le rat [J]. J Agr Food Chem,2005,53 :2941-2946.
[14]Suzuki YA,et al.effet antidiabétique de supplemen- tation à long terme avec siraitia grosvenori on the spontanément diabétique Goto-kakizaki rat[J]. Brit J Nutr,2007,97 :770-775.
[15]Jiang SY,et al.GAP De Siraitia grosvenorii Cul - turé in vitro et établissement de son SOP[J]. Guihaia,2007,27 :867-872.
[16] mon CM,et al. Mode opératoire normalisé sur les cultures de tis Les jeunes plants La multiplication of Siraitia grosvenorii (Swingle)C.Jeffrey[J]. Lishizhen Med Mater Med Res,2008,19 :2092-2094.
[17]Reed J,et Au niveau régional traduction synthetic biology plateforme for Accès rapide à des quantités à l’échelle d’un gramme de nouvelles molécules de type médicament [J]. Metab Eng,2017,42:185-193.
[18]Pawar RS,et al.édulcorants À partir de Plantes avec L’accent est mis sur: Sur stevia rebaudiana(bertoni) et siraitia grosvenorii(swingle) [J]. Anal Bioanal Chem,2013,405 :4397-4407.
[19]Qi XY,et Al.étude d’efficacité sur la poudre de siraitia grosvenori et ses extraits pour réduire la glycémie chez les lapins diabétiques [J]. Food Sci,2003,24:124-127.
[20]Szkudelski T. Le conseil des ministres mécanisme of alloxan and streptozotocine Action dans les cellules b du pancréas du rat [J]. Physiol Res,2001, 50:537-546.
[21]Qi XY,et al.Mogrosides extrait de siraitia grosvenori scav- conteste les radicaux libres in vitro et réduit le stress oxydatif, le sérique Le glucose, et lipides levels in Induit par l’alloxan diabétique mice [J]. Nutr Res,2008,28 :278-284.
[22]Chen SY,et Al.mécanisme de l’intervention du morgroside dans les dommages liés au stress oxydatif de l’îlot pancréatique B Cellule induite par l’acide palmitique [J]. Chin Pharm, 2012,23 :2116-2119.
[23]Chen SY,et al.Progress Dans le mécanisme de stress oxydatif des cellules bêta des îlots et des médicaments thérapeutiques apparentés dans le diabète de type 2 [J]. Chin Pharm, 2011,22:3533-3536.
[24]Zhang LQ,et Al.etude de l’activité antioxydante in vitro d’extraits de siraitia grosvenori.Fruits[J]. Food Sci,2006,27 :213-216.
[25]Qi XY,et al.effet d’un extrait de siraitia grosvenori contenant des mogrosides sur le système immunitaire cellulaire de souris diabétiques de type 1 [J]. Mol Nutr Food Res,2006,50:732-738.
[26] il est CW,et Al. Effet régulateur des saponines fraîches de mangue - steen sur la glycémie [J]. Mod Food Sci Tech,2012,28 :382-386.
[27]Zhou Y,et Al. insuline sécrétion Effets stimulants de mogro- side V v and fruit Extrait de luo Han kuo (siraitia grosvenori) Swingle) fruits Extrait [J]. Acta pharm Sin,2009,44 :1252- 1257.
[28] en MJ,et al.New cucurbitane triterpénoïdes de bitter mel- on avec des propriétés antidiabétiques puissantes associées à activa- tion de ampk[J]. Planta Med,2008,74:913-913.
[29]Zhang LN,et al. allostérique activateur with bénéfique Les effets in Souris db/db [J]. PloS One,2013,8 :e72092.
[30]Chen XB,et al.activateurs ampk potentiels de cucurbitane trit- erpénoïdes de siraitia grosvenoriiswingle[J]. Bioorgue d Chem,2011,19 :5776-5781.
[31]Luo Z,et al. Effet d’activation de l’ampk in vitro et phar- macocinétique in vivo du mogroside v, triterpénoïde de type cucurbitané De siraitia grosvenorii Fruits [J]. Rsc Adv,2016,6 :7034- 7041.
[32]Ag H. : pharmacologie of α-glucosidase Inhibition [J]. Eur Eur J Clin Invest,1994,24:3-10.
[33]nal S,et al inhibition de la α-glucosidase par des extraits aqueux De certains puissant antidiabétique médicinal Herbes [J]. préparation Bio- chem Biote,2005,35 :29-36.
[34]Kumar S,et al. α-glucosidase inhibitors À partir deplants:A natu- ral approach to treat diabetes[J]. Pharmacogn Rev,2011,5:19-28.
[35]Xia X,et Al.effet des extraits de siraitiae fructus de fruits de différentes périodes de croissance sur la glycémie postprandiale chez la souris [J]. Chin J Exp Tradit Med Form,2012,18 :166-170.
[36]Song KJ,et al.effet de l’activation et de l’apoptose du mogroside sur la cellule stellate hépatique [J]. Le menton Tradit Pat Med,2014,36 :481-484.
[37]Zhu, HL,et al.protection Effet de l’ex - trame mogroside on Induit par l’éthanol N ° de catalogue hépatocytes Dommages [J]. J Chin Inst Food Sci Technol,2015,15 (1) :13-18.
[38]Xiao G,et al.protection Effet des mogrosides sur l’expérimentation liver blessure in Souris [J]. Le menton Pharm,2018,19 :163-165.
[39]Wu Y,et al. Étude sur le soulèvement Toux et elimi- nant flegme effects of sténolinine combinées with Mogro - côté En savoir plus Souris [J]. Chin Pharm,2017,28:1755-1757.
[40]Hossen MA,et al.effet De Lo Han Kuo(Siraitia grosvenori Swingle) sur nasale frottement and éraflure comportement in Souris ICR [J]. Biol Pharm Bull,2005,28 :238-241.
[41]Tiwari P,et a.usine Glycosyl-transférases liées au métabolisme secondaire: une mise à jour on En expansion La connaissance and Champs d’application [J]. Biotechnol Adv,2016,34:714-739.
[42] le ministère de la justice L,et al.exploitation the aglycon La promiscuité De la glycosyl-transférase bs-yjic de bacillus subtilis et son application dans Synthèse des glycosides[J]. J Biotechnol,2017,248 :69-76.
[43] Wang R, et Al.Biotransformation des mogrosides[J]. Douceurs :Pharm Biotech Appl,2018,153-165.
[44]Li D,et a.cucurbitane glycosides À partir de Fruits non mûrs de En ce qui concerne Han kuo(Siraitia grosvenori) [J]. Chem Pharm, Bull,2006, 54:1425-1428.
[45]Netala VR, et al.triterpenoïde Saponins :A review on biosyn- thèse,applications et mécanisme de leur action[J]. Int J Pharm Pharm Sci,2015,7 :24-28.
[46]Zhao CL,et al.Key Enzymes de triterpénoïde La saponine biosyn- thèse et l’induction de leurs activités et expositions de gènes dans les plantes [J]. Nat Prod Commun,2010,5 :1147.
[47]Meng JR,et Al.clonage et Analyse séquentielle du pyrophosphate de farnesyl synthase gène in Siraitia grosvenorii [J]. Le menton Tradit herbe Drugs,2011,42 :2512- 2517.
[48]Fett-Neto AG,et al.biosynthèse of plante triterpénoïde Sapo - nines: gènes,enzymes et leur régulation [J]. Mini-Rev Org Chem,2014,11 :292-306.
[49]Zhang J,et al.oxydation of cucurbitadienol catalysé by Cyp87d18 dans la biosynthèse des mogrosides de siraitia gros- venorii[J]. Plant Cell Physiol,2016,57 :1000-1007.
[50]Itkin M,et Al.la voie biosynthétique de Le mogroside v sans sucre, édulcorant de haute intensité de siraitia grosvenorii [J]. P Natl Acad Sci USA,2016,113 :E7619-E7628.
[51]Yoshikawa S,et al.Transglycosylation De mogroside v, un glycoside trit- erpène in siraitia Grosvenori, par cyclodextrine Glu - canotransférase et amélioration des qualités de douceur [J]. J Appl Glycosci,2006,52:247-252.
[52] la loi sur la protection des données L,et al.fonctionnel Caractérisation de cucurbitadienol Synthase et triterpene glycosyltransferase impliqués En biosynthèse of mogrosides from siraitia Grosvenorii [J]. Plant Cell Physiol,2015,56:1172-1182.
[53]Yang XR, et al.Metabolites of siamenoside i and their distribution in rats[J]. Molécules,2016,21 :176.
[54]Yang XW,et al.Biotransformation of mogroside ⊑ par des bactéries intestinales humaines [J]. J pékin Univ :Health Sci,2007,39 :657-662.
[55]Lu LF,et al stabilité de mogroside En savoir plus Le suc gastrique artificiel et son métabolisme in vitro[J]. Guihaia,2015,6:792-795.
[56]Zhou G,et al.le métabolisme d’un produit naturel mogroside v, en santé et de type 2 diabetic Rats [J]. J J J Chromatogr B, 2018,1079 :25-33.
[57]Nong YQ,et al. Un aperçu de la recherche sur l’extraction et l’action pharmacologique des mogrosides[J]. Guangxi J Traditi Chin Med,2008,31 (1) :6-8.
[58]Su XJ9,et al. Études expérimentales sur l’action non-toxique des mogrosides[J]. Food Sci,2005,26(3) :221-224.
59 [59]Xu Q,et al.Study on human human body blood sugar and liver enzymes changes affected by oral mogrosides intake [J]. Food Sci,2007,28 :315-317.
-
Précédent précédent
Comment extraire et séparer Mogroside?
-
Suivant:
Moine extrait de Fruit Mogroside, est-ce sûr?


 Anglais
Anglais français
français espagnol
espagnol russe
russe coréen
coréen japonais
japonais



